Рак желудка
- Общая часть
- Этиология и патогенез
- Клиника и осложнения
- Диагностика
- Лечение
- Прогноз
- Профилактика
- Методы диагностики
Общая часть
Рак желудка – злокачественное новообразование желудка, опухоль, исходящая из эпителия слизистой оболочки желудка.
Рак желудка – полиэтиологичное заболевание, но считается, что большую роль в его возникновении и развитии играет Helicobacter pylori. Клинические проявления включают в себя: потерю аппетита, непроходимость желудка и кровотечения. Диагностируется с помощью эндоскопии с взятием биопсии, рентгенологического исследования, компьютерной томографии и ультразвукового исследования. Лечение, как правило, хирургическое, химиотерапия дает временное улучшение. Долгосрочный прогноз обычно неблагоприятен.
Эпидемиология рака желудка
Во многих странах рак желудка – самая частая злокачественная опухоль.
На долю рака желудка приходится около 15,5% от всех злокачественных новообразований и 20,8% умерших от злокачественных новообразований. По распространенности занимает 4-ое место после рака легкого, молочной железы и колоректального рака.
Аденокарцинома желудка стоит на втором месте как причина смертности от онкозаболеваний в мире. В 2001 году от рака желудка умерло 850,000 людей среди которых 522,000 мужчин и 328,000 женщин. Согласно данным, полученным Всемирной Организацией Здравоохранения, наиболее распространенные формы рака во всем мире (за исключением немеланомных опухолей кожи) это рак легких (12,3%), рак молочной железы (10,4%), и толстого кишечника (9,4%). Среди причин смерти при раковых заболеваниях первые три места занимают соответственно рак легких (17,8%), рак желудка (10,4%) и рак печени (8,8%).
Наблюдаются значительные географические различия в частоте возникновения этого заболевания. Наиболее высокая смертность зафиксирована в Чили, Японии, Южной Америке и странах бывшего СССР.
Мужчины болеют раком желудка в 2 раза чаще женщин.
С возрастом уровень заболеваемости повышается. Наиболее поражаемый возраст – после 60 лет ( в среднем 63 года).
В последние десятилетия отмечается тенденция к снижению заболеваемости раком желудка.
Классификации рака желудка
- По локализации:
- антральный отдел – 60-70%.
- по малой кривизне – 10-15%.
- кардиальный отдел – 8-10%.
- на передней и задней стенках желудка – 2-5%.
- по большой кривизне – 1%.
- на дне желудка – 1%.
- По внешнему виду:
- полипозный (грибовидный).
- блюдцеобразный.
- диффузный.
- язвенно-инфильтративный.
- По микроскопической картине:
- недифференцированный. Мелко– и крупноклеточный рак.
- дифференцированный. Железистый рак (аденокарцинома), фиброзный рак (скирр), смешанные и редкие формы.
Аденокарцинома желудка.
Полип желудка.
Лейомисаркома желудка.
Стадии рака желудка
- Первая стадия – опухоль протяженностью до 3 см, прорастающая слизистую оболочку и подслизистый слой. Метастазы в лимфатические узлы отсутствуют.
- Вторая стадия – опухоль протяженностью более 3 см, но без прорастания в мышечный слой или опухоль любых размеров, прорастающая мышечный слой, но без поражения серозного. Стадия 2А – метастазы в лимфатические узлы отсутствуют. Стадия 2Б – метастазы одиночные (не более 2) в регионарные лимфатические узлы.
- Третья стадия – опухоль любого размера, прорастающая всю стенку желудка или переходящая на пищевод или двенадцатиперстную кишку. Стадия 3А – метастазы в лимфатические узлы отсутствуют. Стадия 3Б – имеются множественные метастазы в регионарных лимфатических узлах.
- Четвертая стадия – опухоль, прорастающая в окружающие органы и ткани или опухоль с метастазами в отдаленные органы.
Классификация TNM
Стадии рака желудка устанавливают по классификации TNM. T (tumor) – опухоль (ее размеры), N (nodulus) – узлы (наличие метасмазов в лимфатических узлах), M (metastasis) – наличие отдаленных метастазов.
- Опухоль T1 проникает в стенку до подслизистой основы.
- Опухоль T2 проникает до субсерозной оболочки.
- Опухоль T3 прорастает серозную оболочку.
- Опухоль T4 распространяется на прилежащие структуры.
- N0 – нет признаков метастатического поражения лимфатических узлов.
- N1 – имеются метастазы в перигастральные лимфатические узлы.
- N2 – имеются метастазы в регионарные лимфатические узлы.
- M0 – метастазы отсутствуют.
- M1 – имеются отдаленные метастазы.
- Стадия I: T1N0, T1N1, T2N0, все – M0.
- Стадия II: T1N2, T2N1,T3N0 , все – M0.
- Стадия III: T2N2, T3N1,T4N0, все – M0.
- Стадия IV: T4N0M0, любые варианты с M1.
Коды по МКБ-10
- С16 – Злокачественное новообразование желудка.
- С16.0 Злокачественное новообразование кардии желудка.
- С16.1 Злокачественное новообразование дна желудка.
- С16.2 Злокачественное новообразование тела желудка.
- С16.3 Злокачественное новообразование преддверия привратника.
- С16.4 Злокачественное новообразование привратника.
- С16.5 Злокачественное новообразование малой кривизны желудка неуточненной части.
- С16.6 Злокачественное новообразование большой кривизны желудка неуточненной части.
- С16.8 Поражение желудка, выходящие за пределы одной и более вышеуказанных локализаций.
- С16.9 Злокачественное новообразование желудка неуточненной локализации.
Этиология и патогенез
Этиология рака желудка
Причина развития рака желудка полностью не ясна.
К возможным этиологическим факторам развития рака желудка относят:
- Характер питания и прием канцерогенных веществ.
- Избыточное потребление поваренной соли.
- Заброс желчи в желудок. Развитие кишечной метаплазии.
- Курение и злоупотребление алкогольными напитками.
- Хронический гастрит, ассоциированный с хеликобактериальной инфекцией. Атрофия и дисплазия, развивающиеся на фоне хронического гастрита, рассматриваются в качестве предраковых изменений. Хеликобактер способствует формированию рецепторов на клетках, чувствительных к воздействию различных канцерогенных веществ, усиливающих пролиферацию клеток, иногда по типу раковой. Язвенная болезнь не является предраковым заболеванием.
- Наличие аденоматозных полипов в желудке.
- Воздействие химических факторов на слизистую оболочку желудка.
- Воздействие физических факторов на организм человека – ионизирующее излучение.
- Повышенное содержание селена в почве.
- Наследственный фактор для рака желудка не достаточно изучен.
- Уровень жизни больного. У лиц с низким социально-экономическим уровнем жизни рак желудка встречается в 5 раз чаще, чем у лиц с благополучными условиями жизни. Ряд исследователей объясняет этот факт тем, что у лиц с низким социально-экономическим уровнем жизни часто имеет место распространение хеликобактериоза с раннего возраста.
Патогенез рака желудка
Патогенез рака желудка не изучен.
На сегодняшний день известно, что рак желудка связан с мутациями генов 53, АРС, k-ras. Потеря гетерозиготности с большой частотой наблюдается на следующих участках хромосом: 17p(локус гена p53), 5q (локус гена АРС) и 18q (локус гена DDC). При раке желудка мутация гена k-ras встречается относительно редко. Как известно,последняя играет большую роль в поддержании опухолевого роста, а появление делеций генов-супрессоров опухолевого роста 17qи 18q происходит обычно на поздних стадиях и служит маркером малигнизации и метастазирования опухоли.
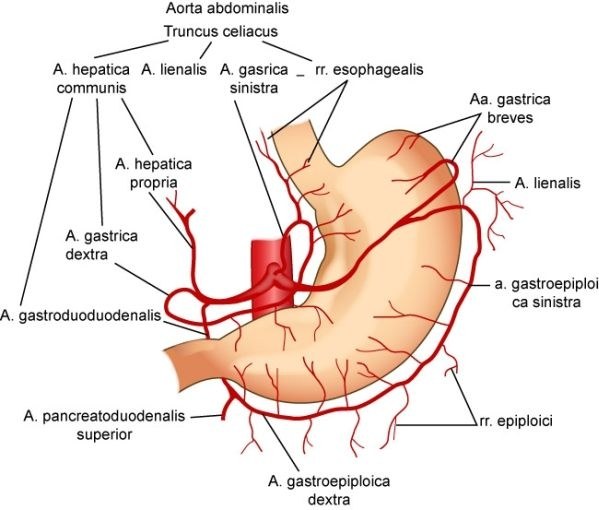
Схема кровоснабжения желудка.
Понимание схемы кровоснабжения желудка помогает предугадать маршруты возможного гематогенного метастазирования. Желудок кровоснабжается чревной артерией. Левая желудочная артерия, ветвь чревной артерии, кровоснабжает верхнюю правую часть желудка. Общая печеночная артерия делится на правую желудочную артерию, снабжающую нижнюю часть желудка, и a. gastroepiploica, снабжающую нижнюю часть большой кривизны.
Зная особенности лимфооттока от желудка, можно предугадать пути возможного распространения метастазов по лимфатическим путям. Основной путь лимфооттока проходит через чревную ось. Малые пути лимфооттока проходят через область селезенки, наджелудочную группу узлов, врата печени и гастродуоденальную область.
Регионарные лимфатические узлы при раке желудка поражаются у 45—65% больных, даже при небольших по диаметру опухо¬лях желудка, и вероятность поражения лимфатических узлов возрастает по мере увеличения инфильтрации стенки желудка. Так, при локализации опухоли в пределах слизистой оболочки метастазы в регионарные лимфатические узлы отмечены у 1,8% больных, при поражении мышечного слоя – у 44,3%, а при распространении опухоли на серозную оболочку желудка регионарные метастазы выявляются у 73,2% больных. После поражения регионарных лимфатических узлов возможно поражение забрюшинных узлов и отдаленное метастазирование. Наиболее часто встречаются отдаленные метастазы в лимфатических узлах левой надключичной области (метастаз Вирхова).
Пример гематогенного пути метастазирования – появление метастазов по системе воротной вены в печени (31,4%), у каждого третьего больного при вторичном поражении печени развивается асцит.
Одновременно возможно метастазирование в кости (0,8%), яичники у женщин (метастаз Крукенберга – 3,4%), брюшину (18,2%) и другие органы.
По В. А. Печатниковой (1967), происхождение некоторых отдаленных метастазов представляется следующим образом. В начале заболевания обычно имеет место ортоградный путь метастазирования, т. е. раковые клетки распространяются по ходу тока лимфы. По мере блокирования лимфоузлов метастазами рака появляются ретроградный лимфоток и ретроградные метастазы (через забрюшинные лимфатические пути – метастазы Крукенберга в яичники, метастазы Шницлера в параректальную клетчатку, метастазы в пупок по круглой связке печени – узелок сестры Мэри Джозеф). При блокировании метастазами парастернальных лимфоузлов лимфа, оттекающая в верхние узлы этой цепочки от нижних глубоких узлов шеи, встречает препятствие, а в надключичных лимфоузлах появляются ретроградно-лимфогенным путем метастазы Вирхова. Происхождение метастазов Вирхова может быть обусловлено и другим путем распространения раковых клеток.
Клиника и осложнения
Специфических симптомов рака желудка не существует. Многое в клинической картине зависит от локализации процесса и стадии заболевания. Часто заболевание протекает бессимптомно до поздних стадий.
При раке желудка могут наблюдаться следующие симптомы:
- Боли в эпигастрии.
- Диспепсия.
- Снижение аппетита вплоть до анорексии.
- Похудание.
- Общая слабость.
- Дисфагия.
- Чувство тяжести после еды.
- Регургитация (срыгивание) во время еды.
- Рвота съеденной за несколько часов или накануне пищей.
- Плохой запах изо рта.
- Отрыжка тухлым.
- На поздних стадиях заболевания истощение и обезвоживание больных.
При наличии нескольких из этих симптомов необходимо обратиться к врачу и провести диагностические исследования с целью исключения или подтверждения онкологического диагноза.
Диагностика
Заподозрить наличие рака желудка возможно при наличии диспептических явлений, снижении массы тела больного и ухудшении общего состояния. При малейшем подозрении на заболевание необходимо провести ЭГДС с биопсией.
Методы диагностики рака желудка
- Сбор жалоб и анамнеза.
- Осмотр больного. Тщательная пальпация пупка, надключичных лимфатических узлов (чаще поражаются левые узлы – вирховские метастазы).
- Эзофагогастродуоденоскопия с биопсией. Важнейшее и обязательное исследование при подозрении на рак желудка.
- Рентгенологические исследования пищевода и желудка.
- Клинический анализ крови. Характерны: Анемия, ускорение СОЭ.
- УЗИ органов брюшной полости. Этот метод помогает исключить наличие метастазов в печени.
- Рентгенография легких. Этот метод помогает исключить наличие метастазов в легких.
- Биохимическое исследование крови. Может наблюдаться неспецифичное повышение активности щелочной фосфатазы, АСТ, АЛТ.
- КТ брюшной полости.
- Диагностическая лапаратомия.
- Ректальное исследование с целью исключения метастазов лимфатических узлов в параректальную клетчатку (шницлеровские метастазы).
- Вагинальное исследование и УЗИ яичников. С целью исключения метастатических опухолей Крукенберга.
- Определение онкомаркеров в крови. Раковоэмбриональный антиген (РЭА) повышается в 45-50% случаев. СА-19-9 повышается в 20% случаев.
- Гистологическое исследование биоптатов слизистой оболочки желудка.
В 90-95% случаев всех злокачественных образований желудка обнаруживается аденокарцинома.Аденокарцинома желудка подразделяется по гистологическим критериям на: тубулярную, папиллярную, муциноидную, перстневидноклеточную, и недифференцированную.
Второе по распространенности новообразовние это лимфома.Гастроинтестинальные стромальные опухоли, обычно классифицируемые как лейомиомы или лейомиосаркомы, составляют 2%.
В остальных случаях диагностируются карциноид (1%), аденоакантомы (1%), и чешуйчатоклеточный рак (1%).
Исследователями были предложены различные способы классификации рака желудка. По системе предложенной Лауреном рак желудка классифицируется на тип I (кишечный) и тип II (диффузный). Эти два типа развития заболевания проявляются у пациентов совершенно по-разному.
- I тип кишечный. Экспансивный, эпидемический, кишечный тип рака желудка. Характеризуется наличием хронического атрофического гастрита, сохраненной функции желез, небольшой инвазивностью и четкими краями. По классификации Лаурена он назван эпидемическим потому, что развивается обычно в результате действия факторов внешней среды, прогноз у него лучше, и отсутствует наследственная предрасположенность.
- II тип диффузный. Диффузный, инфильтративный, эндемический рак. Состоит из разрозненных скоплений клеток со слабой дифференцировкой и нечёткими краями. Края опухоли, которые могли показаться чистыми оперирующими хирургу и исследующему гистологу, часто ретроспективно оказываются обсемененными. Опухоли эндемического типа проникают в ткани желудка на большом протяжении. Этот тип опухолей вероятно не обусловлен влияниями окружающей среды или диеты, чаще развивается у женщин, и поражает относительно молодых пациентов. Отмечена взаимосвязь с генетическими факторами (например Е– кадхерином), группами крови, и наследственной предрасположенностью.
Лечение
Решение о способе лечения принимается на основании стадии опухоли и желания пациента (некоторые пациенты могут предпочесть более или менее радикальную терапию).
Только хирургическое лечение дает ощутимый эффект при раке желудка.
Вспомогательная химиотерапия или комбинированная химиотерапия, а также радиотерапия не оказывают выраженного эффекта при отсутствии хирургического лечения.
Методы лечения
Немедикаментозное лечение
Пациенты с раком желудка должны придерживаться основ лечебного питания.
Хирургическое лечение
Существуют радикальные и паллиативные операции при раке желудка. Радикальными считаются 2 типа операций: субтотальная резекция желудка и гастрэктомия. Чаще всего проводят тотальную гастроэктомию (до здоровых тканей), и эзофагогастрэктомию при опухолях кардии и места перехода пищевода в желудок. При опухолях дистальной части желудка проводят субтотальную гастрэктомию.
Радикальные операции – это удаление большей части или всего желудка и прилежащих лимфатических узлов, оправданы у пациентов с патологическим процессом, ограниченным желудком и региональными лимфатическими узлами (менее 50% пациентов). Рекомендуется иссекать ткани на расстоянии 5 см проксимальнее и дистальнее края опухоли, так как сеть лимфатических сосудов желудка хорошо развита и опухоль склонна к метастазированию. Радикальное лечение показано соматически сохранным больным в возрасте до 75 лет, при отсутствии метастазов – примерно 1/3 всех больных.
При резекции локализованного патологического образования наблюдается 10-летняя средняя выживаемость (без резекции 3-4 года). При сравнении субтотальной и тотальной гастрэктомии при дистальном раке желудка в рандомизированном исследовании существенных различий в склонности к рецидивам, смертности и 5-летней выживаемости выявлено не было.
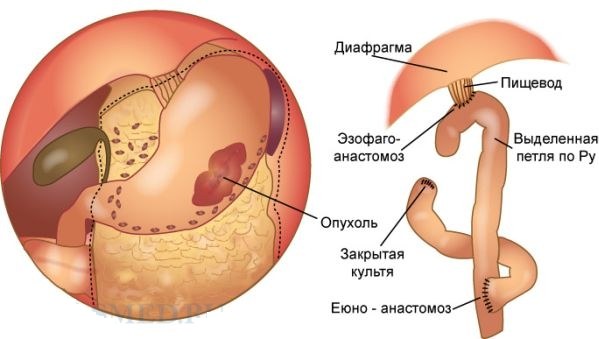
Тотальная гастрэктомия.
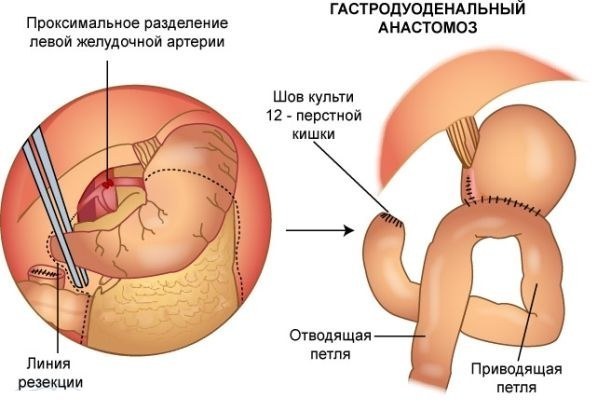
Субтотальная гастрэктомия.
Исходы радикального хирургического лечения
Летальность во время операции – 10%. Показатели послеоперационной смертности в течение 30 дней после хирургической операции при раке желудка значительно снизились за последние 40 лет. По данным большинства крупных центров этот показатель составляет 1-2%.
Процент 5-летней выживаемости после радикальной резекции составляет 60-90% у пациентов при первой стадии заболевания, 30-50% у пациентов со второй стадией, и 10-25% у пациентов с 3-ей стадией заболевания.
К сожалению, только небольшая часть пациентов после радикальных операций полностью излечиваются. У большинства пациентов возникают рецидивы.
Виды рецидивов
Проводилось несколько исследований по изучению видов рецидивов после хирургической резекции, не сопровождавшейся химио– или радиотерапией. Исследования, основанные только на данных физикального обследования, лабораторных исследованиях и визуализирующих методах обследования, обычно дают завышенные показатели отдаленных рецидивов и заниженные показатели труднодиагностируемых рецидивов. Серия реоперационных исследований, проведенная в Университете Миннесоты, позволяет более точно понять схему дальнейшего развития заболевания. При этих исследованиях проводилась хирургическая ревизия пациентов спустя 6 месяцев после первичной операции, и тщательно фиксировались результаты. При этом частота локальных рецидивов составила 67%. Частота возникновения рецидивов в ложе желудка составила 54% всех случаев, в лимфатических узлах– 42%. Приблизительно у 22% пациентов наблюдались отдаленные рецидивы. Приблизительно у 22% пациентов наблюдались признаки отдаленных рецидивов. Рецидивы наблюдались, на месте локальной опухоли, в ложе опухоли, в регионарных лимфатических узлах и отдаленные рецидивы (например, гематогенные метастазы и брюшинное обсеменение). Первичные опухоли, локализовавшиеся в месте перехода пищевода в желудок, обычно метастазировали в печень и легкие. Опухоли с вовлечением пищевода метастазировали в печень.
Осложнения хирургического лечения
В 15-20% больных после операции развиваются постгастрэктомические расстройства.
- В раннем послеоперационном периоде могут возникать следующие осложнения:
- Недостаточность анастомоза.
- Кровотечения.
- Кишечная непроходимость.
- Непроходимость анастомоза.
- Холецистит (часто приводящий к сепсису, без признаков местного воспаления).
- Панкреатит.
- Легочные инфекции.
- Тромбоэмболия.
- К поздним осложнениям относят:
- Демпинг-синдром.
- Диаррея.
- Язва анастомоза.
- Дефицит витамина B 12 .
- Рефлюкс – эзофагит.
- Нарушения костной ткани, чаще всего остеопороз.
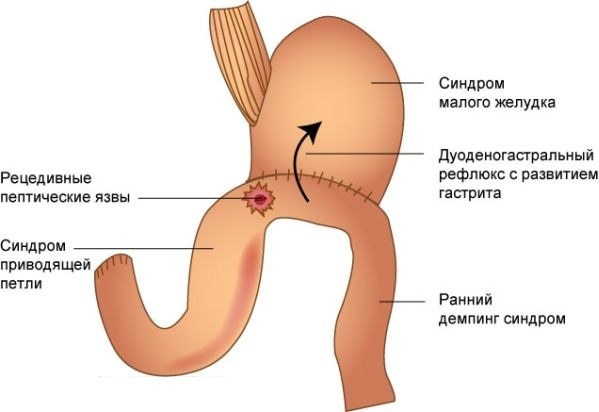
Осложнения гастрэктомии.
Вспомогательная терапия
После проведения хирургического лечения с целью предотвращения рецидивов больным назначается вспомогательная терапия. Учитывая частоту возникновения рецидивов, в мире был проведен ряд исследований по вспомогательной терапии.
Химиотерапия и лучевое лечение проводятся по особым показаниям, в основном для профиактики рецидивов.
Сравнительные данные при проведении предоперационной и постоперационной химиотерапии и постоперационной терапии в комбинации с радиотерапией противоречивы.
Вспомогательная радиотерапия
Цель радиотерапии – предотвратить локальное метастазирование.
Moertel и соавторы, в рандомизированном исследовании пациентов с раком желудка, показали, что при применении радиотерапии в дозе 40 Грей (Гр) или радиотерапии в дозе 40 Гр с использованием 5-фторурацила в качестве радиосенсибилизатора, достоверно улучшаются показатели выживаемости при применении комбинированной терапии.
Британские исследователи рака желудка показали снижение риска возникновения рецидивов у пациентов, которым проводилось послеоперационная радиотерапия, по сравнению с пациентами, которым проводилось только хирургическое лечение.
Было выявлено достоверное увеличение 4-хлетней выживаемости у больных с неоперабильным раком желудка, получавшим комбинированную терапию, по сравнению с группой больных, получавших только химиотерапию. (18 и 6% соответственно). В исследованиях, проведенных в клинике Мэйо, было показано достоверное увеличение выживаемости в группе пациентов получавших постоперационную радиотерапию с 5-фторурацилом, по сравнению с группой, не получавшей вспомогательную терапию (23% и 4% соответственно).
Вспомогательная химиотерапия
Вспомогательная химиотерапия используется с целью радиосенсибилизации и предотвращения системных метастазов. Отдельное проведение химиотерапии малоэффективно. Многочисленные рандомизированные клинические исследования не выявили достоверного улучшения выживаемости при использовании химиотерапии в послеоперационном периоде по сравнению с больными, которым проводилось только хирургическое лечение.
В качестве монотерапии или в комбинации используют фторурацил (5-Фторурацил-Эбеве, Фторурацил-ЛЭНС), доксорубицин, цисплатин, митомицин.
Предоперационная химиотерапия позволяет повысить операбильность опухоли, снизить микрометастазирование, определить чувствительность к химиотерапии и снизить риск местных и системных рецидивов, а также повысить общую выживаемость. В Европейском рандомизированном исследовании было показано достоверное улучшение выживаемости у пациентов получавших 3 цикла предоперационной химиотерапии (эпирубицин, цисплатин, и 5-фторурацил), затем операция и 3 цикла постоперационной химиотерапии по сравнению с пациентами, получавшими только хирургическое лечение. У пациентов, получавших вспомогательную химиорадиотерапию, наблюдалось увеличение длительности периода без рецидивов (с 32% до 49%), а также увеличение общей выживаемости (от 41% до 52%), по сравнению с теми пациентами, которые не получали вспомогательной терапии.
Химиотерапия препаратами платины. Схемы первого ряда выбора:
- Комбинация эпирубицина/цисплатина/ 5-фторурацила.
- Комбинация доцетакселя/цисплатина/5-фторурацила.
- Другие схемы включают иринотекан и цисплатину.
- Возможны комбинации с оксалиплатином и иринотеканом.
Лечение неоперабельных опухолей в терминальной стадии
У большого числа пациента выявляются неоперабельные опухоли с отдаленными метастазами, карциноматоз, неоперабельные печеночные метастазы, метастазы в легких, или инфильтрация органов, не подлежащих резекции. Данной категории больных рекомендовано проводить паллиативную терапию. Средняя продолжительность паллиативной терапии 4-18 месяцев.
В качестве паллиативного лечения, радиотерапия снижает частоту развития кровотечений, степень обструкции, и выраженность болевого синдрома у 50-75% пациентов.
Хирургическая паллиативная терапия включает в себя локальное иссечение, частичную гастрэктомию, тотальную гастрэктомию, наложение гастроинтестинального анастомоза, с целью дать возможность орального приема пищи.
Стандартная схема паллиативной химиотерапии влкючает в себя химиотерапию основанную на применении цисплатина, но результаты слабоутешительны – среднее время начала ухудшения 3-4 месяца и общая выживаемость 6-9 месяцев.
В 2007 году японскими клиницистами получены данные о некотором улучшении этих показателей при применении флюоропиримидина S-1 в качестве монотерапии или в сочетании с цисплатином (S-1 включает в себя 3 компонента: тегафур, предшественник 5-фторурацила; гимерацил, ингибитор распада фторурацила; отерацил (оксанат калия) для предотвращения побочных эффектов со стороны желудочно-кишечного тракта). На данный момент эти результаты проходят проверку в исследованиях, проводящихся в Европе и Северной Америке..
Прогноз
Отдаленные результаты зависят от стадии заболевания, гистологического строения опухоли, характера роста опухоли и состояния иммунной системы организма.
Интраоперационная смертность при радикальных хирургических операциях в крупных научных центрах составляет менее 3%.
5-летняя выживаемость после операции при 1-ой стадии болезни составляет 87-100%, при 2-ой – 70-80%, при 3-ей – около 20%.
При отсутствии метастазов в регионарные лимфатические узлы 5-летняя выживаемость после операции достигается у 50-60% больных, при наличии метастазов только в 10-20% случаев.
Средняя продолжительность жизни неоперированных больных с запущенным раком желудка около 4-5 месяцев.
Ухудшают прогноз локальные рецидивы рака желудка.
Профилактика
- В развитии рака желудка доказана роль табакокурения, избыточного потребления соли, животных жиров, нитросодержащих консервированных продуктов, маринадов, копченостей, дефицит в рационе питания антиоксидантов (фруктов, овощей), а также аскорбиновой кислоты (витамин С). В связи с этим профилактика рака желудка должна предусматривать исключение вредных привычек и поддержание рационального (сбалансированного) питания.
- К профилактическим мерам следует отнести также эрадикацию хеликобактерной инфекции, так как доказана её роль в развитии хронического активного гастрита, кишечной метаплазии, атрофии и рака желудка.
- Следует обеспечить диагностику и лечение рака желудка в ранней стадии его развития с помощью соответствующих диагностических исследований (эндоскопия, прицельная множественная гастробиопсия, крупнокадровая флюорография «здоровых» лиц 50-летнего возраста). К группам повышенного риска относят больных с предраковыми заболеваниями желудка, кровных родственников больных с диффузной формой рака желудка (особенно с А (II) группой крови), лица старше 50 лет со сниженной секрецией желудочного сока.
Методы диагностики
Исследование кодирующих экзонов гена CDH1 на наличие мутаций (в крови)
Определение вариантов первичной структуры 2076С/Т и 160С/А в гене CDH1 (в крови)