Тормозные аминокислоты
Прозоровский В.Б., доктор медицинских наук
Хорошо известно, что важнейший компонент нашей пищи – белки. Хотя углеводы и весьма существенны для обеспечения организма энергией, но они могут получаться и из жиров, и из аминокислот. Жиры тоже не проблема. А вот белки – и мышечные, и белки соединительной ткани, и, главное, ферменты – получаются только из аминокислот. Из них 14 могут синтезироваться в организме, а 8, подобно витаминам, должны поступать в организм человека из пищи. Если во время голода организм, истощив запасы жира и углеводов, для подержания энергетических процессов берётся за белки – беда. У детей возникает отставание в физическом и умственном развитии, у взрослых – голодные отёки, снижение температуры и ослабление всех видов жизнедеятельности.
Человеку нужно всего 120 г белков в сутки, но в растительной пище их маловато, да и усваиваются растительные белки плохо. По моему мнению, мясо, рыба и молочные продукты обязательно должны входить в рацион. Если же в пище недостаёт отдельных аминокислот (пусть даже не из числа незаменимых), то их можно принимать в виде лекарственных препаратов, как, например, глутаминовую кислоту, гистидин. Особенно часто применяется метионин, который совершенно необходим при дистрофических процессах в печени и сердце, и глицин как успокаивающее. (Но о нём мы поговорим позже.)
Гамма-аминомасляная кислота
Долго оставалось неясным, каким же образом обеспечивается снижение общей активности мозга – например, во время сна. Учёные догадывались, что должно существовать вещество, может быть, передатчик нервных импульсов – медиатор, который обеспечивал бы уменьшение активности нервной системы не в отдельных клетках и даже не в нервных ядрах, а вообще в мозгу. И такой универсальный тормозной медиатор был обнаружен. Им оказалась гамма-аминомасляная кислота, которую в дальнейшем мы будем называть сокращённо – ГАМК.
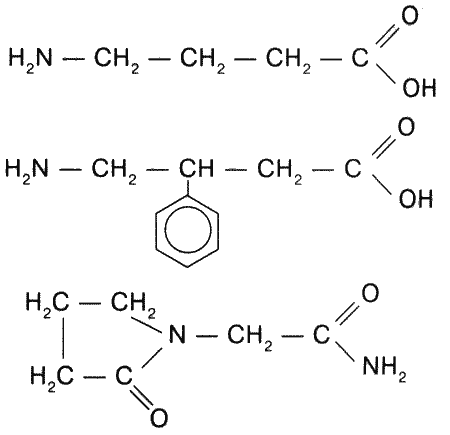
Рис. 1. Структурные формулы гамма-аминомасляной кислоты и её производных: а – гамма-аминомасляная кислота (аминалон, гаммалон); б – фенибут (буфенил); в – пирацетам (ноотропил). Нетрудно заметить, что кольцо ноотропила представляет собой замкнутую молекулу ГАМК
Впервые ГАМК в мозгу обнаружили Ю. Робертс с коллегами (и независимо от них – Йорг Авапара) в 1950 году. Поскольку молекула масляной кислоты имеет цепочку из трёх углеродных атомов (и четвертый – в группе COO), то по систематической номенклатуре кислота должна бы именоваться аминобутановой, но ведь и уксусную кислоту никто не называет этановой (рис. 1).
Строительным материалом для белков служат альфа-аминокислоты: те, у которых аминогруппа присоединена к атому углерода, расположенному рядом с карбоксигруппой. А на что может пригодиться гамма-аминокислота?
Известно, что при раздражении кожи (а также любых других органов чувств) в соответствующих участках коры головного мозга возникают электрические потенциалы, называемые первичными ответами. В 1963 году английский учёный К. Крневич подвёл к одному из нейронов, воспроизводящих первичные ответы, пипетку, заполненную очень слабым раствором ГАМК. Ему впервые удалось установить, что вытекающая из пипетки аминокислота способна полностью подавить возникновение импульсов в чувствительных клетках коры головного мозга. Японские исследователи сделали ещё проще: к поверхности мозга подводили лёгкий электрод, а на него „верхом“ сажали фильтровальную бумажку, смоченную раствором ГАМК. Преимущество такого опыта состояло не только в простоте, а ещё и в том, что амплитуда регистрируемых потенциалов, формируемая не одним, а несколькими нейронами сразу, приблизительно отражает силу воздействия. Концентрация вещества при этом, понятно, требовалась большая, но эффект оказался тем же – потенциалы подавлялись. Позднее подобные опыты были воспроизведены автором этой статьи (рис. 2).
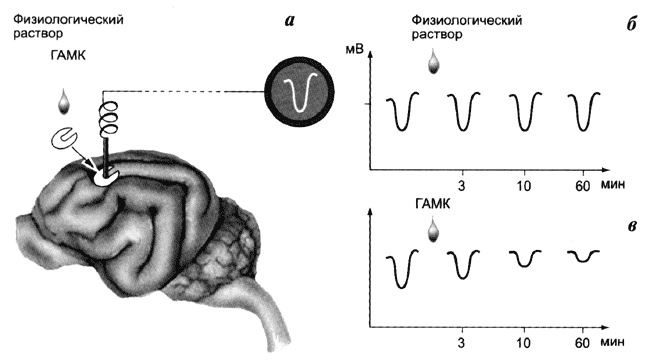
Рис. 2. Торможение первичных ответов в чувствительной зоне коры головного мозга кошек при наложении фильтровальной бумажки, смоченной 1%-ным раствором ГАМК:
а – схема опыта (отведение токов плавающим электродом);
б – первичные ответы после воздействия физиологического раствора;
в – то же после ГАМК.
На вертикальной оси – милливольты, на горизонтальной – минуты. Хорошо видно, как уменьшается со временем амплитуда сигнала
Далее было установлено, что ГАМК может тормозить не только вызванные, но и самостоятельно возникающие потенциалы, как в коре, так и в других участках мозга. При этом ГАМК синтезируется и выделяется именно в тех ядрах мозга, которые ответственны за его торможение. Считается, что ГАМК обеспечивает передачу тормозных импульсов приблизительно в 30–50% нервных контактов. Как она это делает?
Контакты нервных волокон с клетками – синапсы, функционирующие с участием ГАМК, принципиально не отличаются от прочих. ГАМК синтезируется в цитоплазме нейрона и с приходом импульса выделяется в синаптическую щель между окончанием нервов и прилежащим участком оболочки нейрона (рис. 3). Обнаружены и специализированные белки-рецепторы (от лат. recipe – возьми), взаимодействующие с ГАМК. В результате этого взаимодействия в мембране принимающего нейрона открываются каналы, пропускающие внутрь клетки отрицательно заряженные ионы хлора, которые в межклеточной жидкости содержатся в избытке. Проникновение хлора вызывает в клетке состояние гиперполяризации, то есть торможения (напомним, что передача возбуждения происходит за счёт противоположного процесса: деполяризации мембраны нейрона). Сейчас установлено, что рецепторы ГАМК есть также и в кровеносных сосудах, особенно в мозгу.
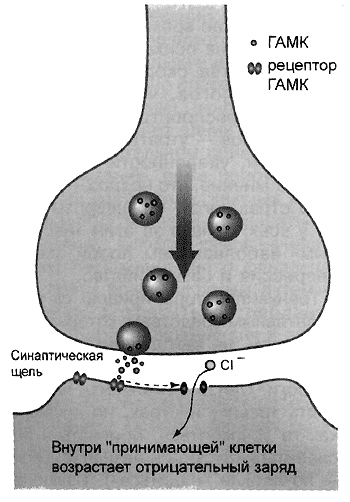
Рис. 3. Схема передачи тормозного импульса в ГАМК-эргическом синапсе. Нервный импульс освобождает ГАМК в синаптическую щель, затем взаимодействие ГАМК с рецептором открывает хлорные каналы. Поступление отрицательных ионов хлора в цитоплазму нейрона вызывает его торможение – утрату чувствительности к раздражениям
Учёные составили карты, на которых указали, где именно ГАМК выступает в роли тормозного медиатора и как велико её значение на каждом участке. Хотя концентрация этой кислоты в разных отделах мозга различна, найти её можно практически везде. Подсчитали примерное общее количество её молекул – и удивились. Оказалось, что мозг содержит ГАМК в значительно больших количествах, чем требуется для осуществления медиаторных функций. Зачем, спрашивается, так много?
Естественно было предположить, что ГАМК выполняет в мозгу ещё какие-то функции. И в самом деле, она оказалась обязательным участником многих обменных процессов. Она воздействует на транспорт и утилизацию глюкозы, на дыхание клеток, на образование в них запасов энергии, повышает устойчивость клеток и мозга в целом к кислородному голоданию, активирует синтез белков. Многообразие физиологических и биохимических функций, выполняемых ГАМК, а также данные о нарушении её образования при некоторых психопатологических и неврологических расстройствах – всё это говорило о её огромном значении. Мимо такой удивительной молекулы фармакологи пройти не могли.
В поисках новых лекарств учёные вспомнили о том, что растения уже миллионы лет назад научились синтезировать соединения, которые успешно блокируют эффекты медиаторов. В случае ГАМК это алкалоиды пикротоксин (содержится в семенах древесных лиан рода Anamirta, которые растут в странах тропической Азии – Индонезии, Индии, Новой Гвинее, на Молуккских островах, а также в различных видах астрагала) и бикукулин (выделен из листьев Dicentre cucullaria семейства дымянковых). Оба эти вещества пытались применять для активации работы мозга, однако они оказались слишком опасными, поскольку уже в ничтожно малых дозах вызывали сильнейшие судороги. (Из анамирты туземцы некогда готовили яд для „химической“ рыбалки и для стрел.) Сейчас для возбуждения дыхательного центра используется синтетический препарат бимегрид, который тоже блокирует эффекты ГАМК, но более избирательно и не столь активно.
Первым лекарством, активирующим рецепторы ГАМК, была сама эта кислота в чистом виде. Её препарат под названием „гаммалон“ был разработан в Японии, а позднее появился точно такой же отечественный, под названием „аминалон“. Несмотря на то что оба препарата используют довольно давно, их лечебные эффекты остаются непонятными. Дело в том, что из-за низкой растворимости в жирах ГАМК почти не поступает из крови в ткань мозга – однако её центральные эффекты не вызывают сомнений и хорошо изучены. Объяснение ценных свойств гаммалона-аминалона способностью ГАМК расширять сосуды кажется неудовлетворительным.
Фармакологам известно, что для повышения проницаемости веществ в мозг через гематоэнцефалический барьер, отделяющий кровь (по сути, водный раствор) от насыщенных липидами клеток мозга, им нужно „привесить“ хорошо растворимый в жирах радикал. Ленинградские фармакологи, в том числе мой друг профессор И.П. Лапин, предложили ввести в молекулу ГАМК фенильный радикал, превративший её в препарат фенибут, который легко преодолевает барьер – и оказывает выраженное тормозное действие (рис. 1)! Сегодня фенибут – распространённый дневной транквилизатор, и, что особенно ценно, он не мешает вождению транспорта.
Со временем удалось установить, что в тканях мозга ГАМК утрачивает аминогруппу, которая замещается гидроксилом. Называется такое вещество гамма-оксимасляной кислотой. Если ввести её непосредственно в кровь, она не только проникает через гематоэнцефалический барьер, но и оказывает на мозг столь сильное тормозное влияние, что её натриевую соль, оксибутират натрия, можно использовать как средство для общей анестезии (точнее, для выключения сознания) при операциях. Вдумайтесь: человек вырабатывает в своём мозгу вещество, способное вызвать состояние наркоза! Как тут не вспомнить про операции под гипнозом?
Второй способ улучшить проникновение молекулы лекарства в ткани мозга – присоединить к ней какое-либо вещество естественного происхождения, например витамин. В частности, препарат пикамилон получен соединением никотиновой кислоты она же PP, с ГАМК. Как и ожидалось, пикамилон расширяет сосуды мозга и оказывает успокаивающее действие при тревоге, страхе, повышенной раздражительности, а также повышает устойчивость к физическим и психическим нагрузкам.
Создание ГАМК-подобных препаратов и изучение их эффектов позволило говорить о существовании двух основных функций ГАМК – медиаторной и метаболической. С медиаторной функцией связано участие ГАМК в регуляции уровня бодрствования, двигательной активности, сосудистого тонуса, поддержании высокого судорожного порога и отчасти улучшении памяти и мышления. Метаболическая функция – это обеспечение мозга энергией, устойчивость к кислородному голоданию и другим вредным воздействиям.
Ноотропные средства
В 1963 году в бельгийской фирме UCB получили соединение, которое представляло собой гамма-аминомасляную кислоту, свёрнутую в кольцо, с некоторыми дополнительными радикалами. При исследовании этого соединения профессор К. Джиурджи и его сотрудники установили, что оно активно улучшает память и облегчает процесс обучения, то есть влияет на высшие интеллектуальные функции мозга. Поскольку по-гречески мышление и разум – noos, а сродство – tropos, новое лекарство получило название „ноотропил“. А в 1972 году появился термин „ноотропные средства“.
Согласно определению экспертов ВОЗ ноотропные препараты активируют способность к обучению, улучшают память и умственную деятельность, а также повышают устойчивость мозга к агрессивным воздействиям.
В России ноотропил выпускается под названием „пирацетам“, а по всему миру более чем под 30 наименованиями – лишнее свидетельство его необычайной популярности. Показания к его применению – нарушения памяти, снижение концентрации внимания, изменения настроения, расстройства поведения и мышления при болезнях сосудов, травмах и склерозе мозга, а также расстройства психики при хроническом алкоголизме. Препарат хорошо переносится, однако у некоторых людей вызывает неожиданные реакции: возбуждение или, наоборот, сонливость, иногда головокружение, а иногда повышение сексуальности.
На сегодня группа ноотропных средств не имеет жёстко очерченных границ. Кроме уже упомянутых аминалона, фенибута и пикамилона, к ней относят также деонол (нооклерин), идебенон, меклофеноксат, никотиноил-ГАМК и пантогам. Всё это препараты метаболические и в какой-то мере антиоксидантные. Условно к ноотропным средствам причисляют препараты, обладающие выраженной способностью вызывать расширение сосудов мозга: винпоцетин (кавинтон), компламин, трентал, циннаризин и т. п. Ноотропными могут считаться также кофеин и некоторые витамины: B6, B15, BC ;и B12.
Если рассматривать ноотропное действие как таковое, то можно указать, что в его основе лежат три характерных свойства (которые у разных препаратов выражены в разной степени): во-первых, они восстанавливают баланс между возбудительными и тормозными процессами в мозгу, во-вторых, активируют обмен и энергетические процессы в нервных клетках, в-третьих, повышают выносливость нейронов при кислородном голодании и мембранотоксических воздействиях.
В последние годы представление о ноотропных средствах несколько изменилось. Предполагается, что следующее поколение препаратов этой группы будет не только активировать высшие интегративные функции мозга, но также восстанавливать нарушения памяти и мыслительных процессов, снижать возникающие при разного рода поражениях нервной системы дефициты и повышать сопротивляемость организма. Эти средства преобразят жизнь человечества, избавив его от последствий болезней мозга и обеспечив активную старость. А возможно, и позволят лечить врождённое или приобретённое слабоумие.
ГАМК-рецепторы обладают очень интересной особенностью: они облеплены другими рецепторами, которые также регулируют процесс торможения, как через ГАМК-рецепторы, так и самостоятельно. Среди этих „спутников“ рецепторы барбитуратов, алкоголя и, главное, бензодиазепинов – на сегодня одни из самых распространённых и ценных препаратов с транквилизаторным, миорелаксантным, атарактическим, противосудорожным и снотворным действием. Им придётся посвятить отдельный раздел.
Бензодиазепины – основные транквилизаторы
Слово „бедлам“ в значении „полный беспорядок“ происходит от названия самой крупной психиатрической больницы XIV века в Лондоне. Там действительно творилось нечто совершенно беспорядочное: больных с разными формами психозов содержали в общих залах. Некоторые из них вели себя настолько буйно, что становились опасными для окружающих. Тогда их сажали в специальное кресло, вроде электрического стула, к которому привязывали не только руки и ноги, но и голову несчастного. Больной, безуспешно пытаясь вырваться из пут, постепенно утомлялся и стихал, успокаивался. Такие стулья назывались транквилизаторами (от лат. tranquillo – успокаиваю). Вот откуда пошёл этот распространённый ныне термин.
В настоящее время транквилизаторами лечат не психозы, а неврозы – это лекарства скорее из арсенала невропатологов, чем психиатров. Наиболее распространённые причины неврозов – утрата чувства защищённости, уверенности в будущем. Бытует мнение, что невроз – это „ничего страшного“, что неврозы бывают у всех, однако за этим „нестрашным“ заболеванием порой следуют депрессия и самоубийство.
Транквилизаторы пришли на смену седативным средствам, которые давали людям, не находящим себе места от возбуждения, беспокойства или тревоги. Они, к сожалению, не могли снять тревогу и страх, но позволяли как-то успокоиться, присесть и расслабиться (отсюда и название: sedere – по-латыни „садиться“). Излюбленными седативными средствами были бром и барбитураты, вызывающие тотальное торможение в мозгу, которые, конечно, не восстанавливали здоровья и были далеко не безвредны. Аналогичным образом, только слабее, действуют лекарственные травы: валериана, пион и пассифлора.
В начале 60-х годов появился первый бензодиазепин – либриум (элениум), который сразу заинтересовал врачей всех специальностей. Особенно привлекательными были его центральная миорелаксантная (расслабляющая скелетную мускулатуру) и противосудорожная активность. В настоящее время бензодиазепинов существует множество. К противотревожным транквилизаторам относят элениум (в русском варианте хлозепид), сибазон (диазепам, реланиум, седуксен), нозепам (тазепам) и феназепам, обладающие выраженным анксиолитическим (противотревожным, от anxius – тревожный, охваченный страхом) и седативным действием. Бензодиазепины без седативно-гипнотического эффекта называют дневными транквилизаторами. К ним относится мезапам (он же рудатель).
Все эти препараты переносятся хорошо, однако у многих из них описаны побочные эффекты: головная боль, сонливость, нарушение потенции, снижение скорости реакции, способность усиливать действие алкоголя, вызывая патологическое опьянение с потерей сознания. Особенно опасен в этом отношении феназепам, эффект которого может длиться от одних до четырёх суток. При длительном приёме наступает привыкание, реже пристрастие, ухудшение настроения, человек начинает принимать новые препараты из этой группы… Словом, лучше начинать лечение бессонницы не с феназепама, а пойти более сложным путём – например, сократить потребление кофе во второй половине дня и перед сном заварить травяной чай: вдруг таблетка и не понадобится?
Сейчас Россия закупает за рубежом сравнительно новый препарат гидазепам, транквилизаторный эффект которого сочетается с активирующим действием. Он эффективен и при лечении мигрени. Альпрозалам интересен своим антидепрессивным действием. На мой взгляд, именно эти препараты должны бы пользоваться особым спросом, однако этого нет. Вероятно, потому, что их названия не мелькают на красочных плакатах и не повторяются в рекламных роликах.
Глицин как мягкий транквилизатор
Второй заменимой тормозной аминокислоте, глицину, выпал не слишком громкий, но заслуженный успех, хотя он всего-навсего аминоуксусная кислота. В тканях мозга его немного, но это небольшое количество совершенно необходимо. Будучи тормозным медиатором, глицин препятствует распространению импульса, пришедшего по чувствительным задним корешкам спинного мозга, в другую его половину и другие сегменты. Непревзойдённые по активности природные антагонисты глицина, которые связываются с его рецепторами, – столбнячный токсин и алкалоид стрихнин, содержащийся в рвотных орешках Nux vomica, они же плоды святого Игнация. (Стрихнин – хорошо известный яд, а рвотные орешки – одно из самых любимых лекарств у гомеопатов.) Если блокируется действие глицина, то малейшее раздражение вызывает тоническое сокращение мышц всего тела, которое принимает типичную при отравлении стрихнином или столбняке позу опистотонуса: выгибание с опорой на затылок и пятки. В современной научной медицине стрихнин используется редко. А вот глицин завоёвывает всё большую популярность
В клинике подтверждено, что он (при сублингвальном применении) не только усиливает действие противо-судорожных средств, но и ускоряет засыпание, обладает антиоксидантным, противострессорным, транквилизирующим и ноотропным действием, блокируя гипофиз-адреналовую систему.
Согласно клиническим данным, глицин подавляет раздражительность и делает поведение более разумным. В то же время он имеет сходство с транквилизаторами только по седативному эффекту, а по всем остальным пунктам им противоположен. Так, он не оказывает миорелаксантного действия, ослабляет эффект алкоголя, не вызывает зависимости, повышает скорость реакций, усиливает умственную работоспособность, с увеличением дозы его эффект снижается. Глицин не только не мешает водить машину, но рекомендован водителям!
Положим, клинике не всегда можно доверять. Но есть и весьма авторитетные экспериментальные данные в пользу того, что на модели гипоксии мозга с возникновением инфаркта глицин его предупреждает эффективней пирацетама. При этом увеличивается оборот ГАМК, повышается или нормализуется содержание основных медиаторов мозга во многих его отделах, особенно в очаге ишемии. Журнал „Физиология человека“ (2001) сообщает, что после трёхнедельного приёма глицина два раза в день регистрируется увеличение скорости мыслительных процессов.
Сегодня показаниями к применению глицина считаются стрессовые состояния, психоэмоциональное напряжение, повышенная возбудимость, эмоциональная лабильность, неврозы, вегетососудистая дистония, последствия черепно-мозговой травмы, энцефалопатии, в том числе алкогольные, нарушения сна… Настоящее чудо – такое действие обычной аминокислоты, которую мы потребляем с пищей и вырабатываем в собственном организме. Может быть, именно такие лекарства откроют людям путь к здоровью и долголетию.
„Химия и жизнь – XXI век“