Нестероидные противовоспалительные средства
Методическое пособие
Авторы:
Л. С. Страчунский
профессор, заведующий кафедрой клинической фармакологии Смоленской государственной медицинской академии.
С. Н. Козлов
доцент кафедры клинической фармакологии Смоленской государственной медицинской академии.
Рецензенты:
В. Г. Кукес
профессор, член-корреспондент РАМН, заведующий кафедрой клинической фармакологии Московской медицинской академии им. И.М. Сеченова.
В. И. Петров
профессор, заведующий кафедрой клинической фармакологии Волгоградской государственной медицинской академии.
Содержание
- Предисловие
- Введение
- Фармакодинамика
- Фармакокинетика
- Показания к применению
- Противопоказания
- Предупреждения
- Нежелательные реакции
- Меры контроля при длительном применении
- Правила назначения и дозирования
- Лекарственные взаимодействия
- Безрецептурное применение НПВС
- Характеристика отдельных препаратов
- НПВС с выраженной противовоспалительной активностью
- Ацетилсалициловая кислота (аспирин)
- Лизинмоноацетилсалицилат
- Дифлунизал
- Фенилбутазон
- Клофезон
- Индометацин
- Сулиндак
- Этодолак
- Диклофенак-натрий
- Диклофенак-калий
- Пироксикам
- Теноксикам
- Лорноксикам
- Мелоксикам
- Набуметон
- Ибупрофен
- Напроксен
- Напроксен-натрий
- Флурбипрофен
- Кетопрофен
- Тиапрофеновая кислота
- Фенопрофен
- Целекоксиб
- НПВС со слабой противовоспалительной активностью
- Мефенамовая кислота
- Этофенамат
- Метамизол (дипирон)
- Аминофеназон
- Пропифеназон
- Фенацетин
- Парацетамол (ацетаминофен)
- Кеторолак
- Комбинированные препараты
- Саридон
- Томапирин
- Томапирин С
- Цитрамон П
- Алка-Зельтцер
- Форталгин Ц
- Пливалгин
- Реопирин
- Баралгин
- Артротек
- Список литературы
ПРЕДИСЛОВИЕ
Настоящее руководство является первым в серии "Клиническая фармакология – врачу", намеченной к выпуску сотрудниками кафедры клинической фармакологии Смоленской государственной медицинской академии. Первоначально оно планировалось в более сокращенном варианте как учебное пособие для студентов. Но по мере подготовки его к печати была накоплена обширная информация, выходящая за рамки академической программы и, в то же время, имеющая существенный практический интерес.
Нестероидные противовоспалительные препараты занимают одно из первых мест по частоте клинического использования. Это объясняется их действием против боли, воспаления и повышенной температуры тела, то есть симптомов, сопровождающих многие заболевания. За последние годы арсенал нестероидных противовоспалительных средств пополнился значительным числом новых лекарств, причем поиск ведется в направлении создания препаратов, сочетающих высокую эффективность с улучшенной переносимостью.
В руководстве представлена современная классификация нестероидных противовоспалительных препаратов. Рассматриваются новейшие, полученные в контролируемых клинических исследованиях сведения по их фармакодинамике, фармакокинстике и лекарственному взаимодействию, общие принципы клинического применения. Особое внимание уделено нежелательным реакциям, факторам их риска, методам профилактики и коррекции. Включены препараты, которые разрешены для клинического использования в России, а также препараты, прошедшие последнюю фазу клинических испытаний и "стоящие на пороге" регистрации. Подчеркиваются отличительные, имеющие практическое значение, особенности их действия, применения у взрослых и детей.
Руководство предназначено для практических врачей разных специальностей, фармакологов и студентов медицинских вузов.
Во второе издание включена новая информация, касающаяся особенностей клинического применения кеторолака, гастротоксичности аспирина, методов улучшения переносимости нестероидных противовоспалительных средств.
Л.С. Страчунский, С.Н. Козлов
ВВЕДЕНИЕ
Нестероидные противовоспалительные средства (НПВС) представляют собой группу лекарственных средств, которые широко применяются в клинической практике, причем многие из них можно купить без рецепта. Более тридцати миллионов людей в мире ежедневно принимают НПВС, причем 40% этих пациентов имеют возраст старше 60 лет (1). Около 20% стационарных больных получают НПВС.
Большая "популярность" НПВС объясняется тем, что они обладают противовоспалительным, анальгезирующим и жаропонижающим эффектами и приносят облегчение больным с соответствующими симптомами (воспаление, боль, лихорадка), которые отмечаются при многих заболеваниях.
За последние 30 лет количество НПВС значительно возросло и в настоящее время данная группа насчитывает большое число препаратов, отличающихся по особенностям действия и применения.
НПВС классифицируются в зависимости от выраженности противовоспалительной активности и химической структуры (табл. 1). В первую группу включены препараты с выраженным противовоспалительным действием. НПВС второй группы, оказывающие слабый противовоспалительный эффект, часто обозначаются терминами "ненаркотические анальгетики" или "анальгетики-антипиретики".
С практической точки зрения важным является то, что препараты, относящиеся к одной и той же группе и даже близкие по химической структуре, несколько различаются как по силе эффекта, так и по частоте развития и характеру нежелательных реакций. Так, среди НПВС первой группы наиболее мощной противовоспалительной активностью обладают индометацин и диклофенак, а наименьшей – ибупрофен. Индометацин, являющийся производным индолуксусной кислоты, более гастротоксичен, чем этодолак, также относящийся к данной химической группе. Клиническая эффективность препарата может зависеть от вида и особенностей течения заболевания у конкретного больного, а также от его индивидуальной реакции.
Таблица 1. Классификация НПВС по активности и химической структуре
| НПВС с выраженной противовоспалительной активностью | |
|---|---|
| Кислоты | |
| Салицилаты | Ацетилсалициловая кислота (аспирин) Дифлунизал Лизинмоноацетилсалицилат |
| Пиразолидины | Фенилбутазон |
| Производные индолуксусной кислоты | Индометацин Сулиндак Этодолак |
| Производные фенилуксусной кислоты | Диклофенак |
| Оксикамы | Пироксикам Теноксикам Лорноксикам Мелоксикам |
| Производные пропионовой кислоты | Ибупруфен Напроксен Флурбипрофен Кетопрофен Тиапрофеновая кислота |
| Некислотные производные | |
| Алканоны | Набуметон |
| Производные сульфонамида | Нимесулид Целекоксиб Рофекоксиб |
| НПВС со слабой противовоспалительной активностью | |
| Производные антраниловой кислоты | Мефенамовая кислота Этофенамат |
| Пиразолоны | Метамизол Аминофеназон Пропифеназон |
| Производные парааминофенола | Фенацетин Парацетамол |
| Производные гетероарилуксусной кислоты | Кеторолак |
ФАРМАКОДИНАМИКА
Механизм действия
Главным и общим элементом механизма действия НПВС является угнетение синтеза простагландинов (ПГ) из арахидоновой кислоты путем ингибирования фермента циклооксигеназы (ПГ-синтетазы) (рис. 1).
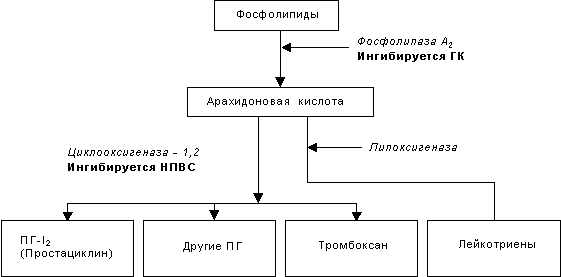
Рис. 1. Метаболизм арахидоновой кислоты
ПГ имеют разностороннюю биологическую активность:
а) являются медиаторами воспалительной реакции: вызывают локальное расширение сосудов, отек, экссудацию, миграцию лейкоцитов и другие эффекты (в основном ПГ-Е2 и ПГ-I2);
6) сенсибилизируют рецепторы к медиаторам боли (гистамину, брадикинину) и механическим воздействиям, понижая порог болевой чувствительности;
в) повышают чувствительность гипоталамических центров терморегуляции к действию эндогенных пирогенов (интерлейкина-1 и других), образующихся в организме под влиянием микробов, вирусов, токсинов (главным образом – ПГ-Е2).
В последние годы было установлено, что существуют, как минимум, два изофермента циклооксигеназы, которые ингибируются НПВС. Первый изофермент – ЦОГ-1 (СОХ-1 – англ.) – контролирует выработку простагландинов, регулирующий целостность слизистой оболочки желудочно-кишечного тракта, функцию тромбоцитов и почечный кровоток, а второй изофермент – ЦОГ-2 – участвует в синтезе простагландинов при воспалении. Причем, ЦОГ-2 в нормальных условиях отсутствует, а образуется под действием некоторых тканевых факторов, инициирующих воспалительную реакцию (цитокины и другие). В связи с этим предполагается, что противовоспалительное действие НПВС обусловлено ингибированием ЦОГ-2, а их нежелательные реакции – ингибированием ЦОГ, классификация НПВС по селективности в отношении различных форм циклооксигеназы представлена в таблице 2. Соотношение активности НПВС в плане блокирования ЦОГ-1/ЦОГ-2 позволяет судить об их потенциальной токсичности. Чем меньше эта величина, тем более селективен препарат в отношении ЦОГ-2 и, тем самым, менее токсичен. Например, для мелоксикама она составляет 0,33, диклофенака – 2,2, теноксикама – 15, пироксикама – 33, индометацина – 107.
Таблица 2. Классификация НПВС по селективности в отношении различных форм циклооксигеназы
(Drugs Therapy Perspectives, 2000, с дополнениями)
| Выраженная селективность в отношении ЦОГ-1 | Аспирин Индометацин Кетопрофен Пироксикам Сулиндак |
| Умеренная селективность в отношении ЦОГ-1 | Диклофенак Ибупрофен Напроксен и др. |
| Примерно равноценное ингибирование ЦОГ-1 и ЦОГ-2 | Лорноксикам |
| Умеренная селективность в отношении ЦОГ-2 | Этодолак Мелоксикам Нимесулид Набуметон |
| Выраженная селективность в отношении ЦОГ-2 | Целекоксиб Рофекоксиб |
Другие механизмы действия НПВС
Противовоспалительное действие может быть связано с торможением перекисного окисления липидов, стабилизацией мембран лизосом (оба этих механизма предупреждают повреждение клеточных структур), уменьшением образования АТФ (снижается энергообеспечение воспалительной реакции), торможением агрегации нейтрофилов (нарушается высвобождение из них медиаторов воспаления), торможением продукции ревматоидного фактора у больных ревматоидным артритом. Анальгезирующий эффект в определенной степени связан с нарушением проведения болевых импульсов в спинном мозге (метамизол).
Основные эффекты
Противовоспалительный эффект
НПВС подавляют преимущественно фазу экссудации. Наиболее мощные препараты – индометацин, диклофенак, фенилбутазон – действуют также на фазу пролиферации (уменьшая синтез коллагена и связанное с этим склерозирование тканей), но слабее, чем на экссудативную фазу. На фазу альтерации НПВС практически не влияют. По противовоспалительной активности все НПВС уступают глюкокортикоидам, которые, ингибируя фермент фосфолипазу А2, тормозят метаболизм фосфолипидов и нарушают образование как простагландинов, так и лейкотриенов, также являющихся важнейшими медиаторами воспаления (рис. 1).
Анальгезирующий эффект
В большей степени проявляется при болях слабой и средней интенсивности, которые локализуются в мышцах, суставах, сухожилиях, нервных стволах, а также при головной или зубной боли. При сильных висцеральных болях большинство НПВС менее эффективны и уступают по силе анальгезирующего действия препаратам группы морфина (наркотическим анальгетикам). В то же время, в ряде контролируемых исследований показана достаточно высокая анальгетическая активность диклофенака, кеторолака, кетопрофена, метамизола при коликах и послеоперационных болях. Эффективность НПВС при почечной колике, возникающей у больных мочекаменной болезнью, во многом связана с торможением продукции ПГ-E2 в почках, снижением почечного кровотока и образования мочи. Это ведет к уменьшению давления в почечных лоханках и мочеточниках выше места обструкции и обеспечивает длительный анельгезирующий эффект. Преимуществом НПВС перед наркотическими анальгетиками является то, что они не угнетают дыхательный центр, не вызывают эйфорию и лекарственную зависимость, а при коликах имеет значение еще и то, что они не обладают спазмогенным действием.
Жаропонижающий эффект
НПВС действуют только при лихорадке. На нормальную температуру тела не влияют, чем отличаются от "гипотермических" средств (хлорпромазин и другие).
Антиагрегационный эффект
В результате ингибирования ЦОГ-1 в тромбоцитах подавляется синтез эндогенного проагреганта тромбоксана. Наиболее сильной и длительной антиагрегационной активностью обладает аспирин, который необратимо подавляет способность тромбоцита к агрегации на всю продолжительность его жизни (7 дней). Антиагрегационный эффект других НПВС слабее и является обратимым. Селективные ингибиторы ЦОГ-2 не влияют на агрегацию тромбоцитов.
Иммуносупрессивный эффект
Выражен умеренно, проявляется при длительном применении и имеет "вторичный" характер: снижая проницаемость капилляров, НПВС затрудняют контакт иммунокомпетентных клеток с антигеном и контакт антител с субстратом.
ФАРМАКОКИНЕТИКА
Все НПВС хорошо всасываются в желудочно-кишечном тракте. Практически полностью связываются с альбуминами плазмы, вытесняя при этом некоторые другие лекарственные средства (см. главу "Лекарственные взаимодействия"), а у новорожденных – билирубин, что может привести к развитию билирубиновой энцефалопатии. Наиболее опасны в этом отношении салицилаты и фенилбутазон. Большинство НПВС хорошо проникают в синовиальную жидкость суставов. Метаболизируются НПВС в печени, выделяются через почки.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
1. Ревматические заболевания
Ревматизм (ревматическая лихорадка), ревматоидный артрит, подагрический и псориатический артриты, анкилозирующий спондилит (болезнь Бехтерева), синдром Рейтера.
Следует учитывать, что при ревматоидном артрите НПВС оказывают только симптоматический эффект, не влияя на течение заболевания. Они не способны приостановить прогрессирование процесса, вызвать ремиссию и предупредить развитие деформации суставов. В то же время, облегчение, которое НПВС приносят больным ревматоидным артритом, настолько существенно, что ни один из них не может обойтись без этих препаратов. При больших коллагенозах (системная красная волчанка, склеродермия и другие) НПВС часто малоэффективны.
2. Неревматические заболевания опорно-двигательного аппарата
Остеоартроз, миозит, тендовагинит, травма (бытовая, спортивная). Нередко при этих состояниях эффективно применение местных лекарственных форм НПВС (мази, кремы, гели).
3. Неврологические заболевания. Невралгия, радикулит, ишиас, люмбаго.
4. Почечная, печеночная колика.
5. Болевой синдром различной этиологии, в том числе, головная и зубная боль, послеоперационные боли.
6. Лихорадка (как правило, при температуре тела выше 38,5°С).
7. Профилактика артериальных тромбозов.
8. Дисменорея.
НПВС применяют при первичной дисменорее для купирования болевого синдрома, связанного с повышением тонуса матки вследствие гиперпродукции ПГ-F2a. Помимо анальгезирующего действия НПВС уменьшают объем кровопотери.
Хороший клинический эффект отмечен при применении напроксена, и особенно его натриевой соли, диклофенака, ибупрофена, кетопрофена. НПВС назначают при первом появлении болей 3-дневным курсом или накануне месячных. Нежелательные реакции, учитывая кратковременный прием, отмечаются редко.
ПРОТИВОПОКАЗАНИЯ
НПВС противопоказаны при эрозивно-язвенных поражениях желудочно-кишечного тракта, особенно в стадии обострения, выраженных нарушениях функции печени и почек, цитопениях, индивидуальной непереносимости, беременности. При необходимости, наиболее безопасными (но не перед родами!) являются небольшие дозы аспирина (3).
Индометацин и фенилбутазон не следует назначать амбулаторно лицам, профессии которых требуют повышенного внимания.
ПРЕДУПРЕЖДЕНИЯ
НПВС должны с осторожностью назначаться больным бронхиальной астмой, а также лицам, у которых ранее выявлялись нежелательные реакции при приеме любых других НПВС.
Для больных гипертензией или сердечной недостаточностью следует выбирать те НПВС, которые в наименьшей степени влияют на почечный кровоток.
У лиц пожилого возраста необходимо стремиться к назначению минимальных эффективных доз и коротких курсов НПВС.
НЕЖЕЛАТЕЛЬНЫЕ РЕАКЦИИ
Желудочно-кишечный тракт
Основным негативным свойством всех НПВС является высокий риск развития нежелательных реакций со стороны желудочно-кишечного тракта. У 30-40% больных, получающих НПВС, отмечаются диспептические расстройства, у 10-20% – эрозии и язвы желудка и двенадцатиперстной кишки, у 2-5% – кровотечения и перфорации (4).
В настоящее время выделен специфический синдром – НПВС-гастродуоденопатия (5). Он лишь отчасти связан с локальным повреждающим влиянием НПВС (большинство из них – органические кислоты) на слизистую и в основном обусловлен ингибированием изофермента ЦОГ-1 в результате системного действия препаратов. Поэтому гастротоксичность может иметь место при любом пути введения НПВС.
Поражение слизистой желудка протекает в 3 стадии:
1) торможение синтеза простагландинов в слизистой;
2) уменьшение опосредованной простагландинами выработки защитной слизи и бикарбонатов;
3) появление эрозий и язв, которые могут осложняться кровотечением или перфорацией.
Повреждение чаще локализуется в желудке, преимущественно в антральном или препилорическом отделе. Клинические симптомы при НПВС-гастродуоденопатии почти у 60% больных, особенно пожилых, отсутствуют, поэтому диагноз во многих случаях устанавливают при фиброгастродуоденоскопии. В то же время, у многих пациентов, предъявляющих диспепсические жалобы, повреждения слизистой не выявляется. Отсутствие клинической симптоматики при НПВС-гастродуоденопатии связывают с анальгезирующим действием препаратов. Поэтому больные, в особенности пожилого возраста, у которых при длительном приеме НПВС не отмечается нежелательных явлений со стороны желудочно-кишечного тракта, рассматриваются как группа повышенного риска развития серьезных осложнений НПВС-гастродуоденопатии (кровотечение, тяжелая анемия) и требуют особо тщательного контроля, включающего эндоскопическое исследование (1).
Факторы риска гастротоксичности: женщины, возраст старше 60 лет, курение, злоупотребление алкоголем, семейный язвенный анамнез, сопутствующие тяжелые сердечно-сосудистые заболевания, сопутствующий прием глюкокортикоидов, иммуносупрессантов, антикоагулянтов, длительная терапия НПВС, большие дозы или одновременный прием двух или более НПВС. Наибольшую гастротоксичность имеют аспирин, индометацин и пироксикам (1).
Методы улучшения переносимости НПВС.
I. Одновременное назначение препаратов, защищающих слизистую оболочку желудочно-кишечного тракта.
По данным контролируемых клинических исследований, высокой эффективностью обладает синтетический аналог ПГ-Е2 – мизопростол, прием которого позволяет предупредить развитие язв как в желудке, так и в двенадцатиперстной кишке (табл. 3). Выпускаются комбинированные препараты, в состав которых входят НПВС и мизопростол (см. ниже).
Таблица 3. Защитный эффект различных препаратов в отношении НПВС-индуцированных язв желудочно-кишечного тракта (По Champion G.D. и соавт., 1997 (1) с дополнениями)
| Препарат | Локализация язвы | |
|---|---|---|
| Желудок | Двенадцатиперстная кишка | |
| Н2-блокаторы | 0 * | + |
| Омепразол | + | + |
| Сукральфат | 0 | – |
| Мизопростол | + | + |
+ профилактический эффект
0 отсутствие профилактического эффекта
– эффект не уточнен
* по последним данным, фамотидин эффективен в высокой дозе
Ингибитор протонного насоса омепразол имеет примерно такую же эффективность, как и мизопростол, но лучше переносится, быстрее устраняет рефлюксы, болевой синдром и нарушения пищеварения.
Н2-блокаторы способны предотвратить образование дуоденальных язв, но, как правило, неэффективны в отношении язв желудка. Однако есть данные, что высокие дозы фамотидина (40 мг два раза в день) снижают частоту развития и желудочных и дуоденальных язв.
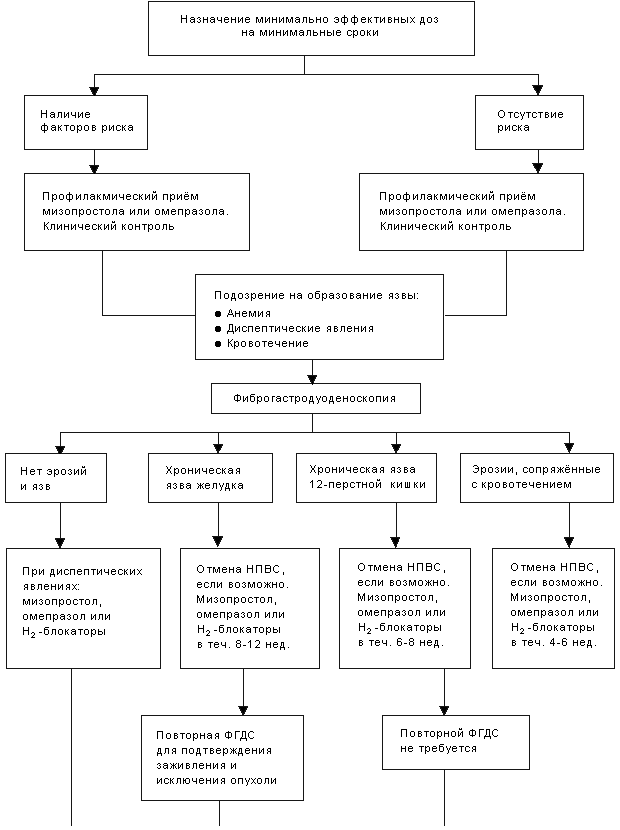
Рис. 2. Алгоритм профилактики и лечения НПВС-гастродуоденопатии.
По Loeb D.S. и соавт., 1992 (5) с дополнениями.
Цитопротекторный препарат сукральфат не уменьшает риск развития язв желудка, его эффект в отношении язв двенадцатиперстной кишки до конца не определен.
II. Изменение тактики применения НПВС, которое предполагает (а) снижение дозы; (б) переход на парентеральное, ректальное или местное введение; (в) прием кишечно-растворимых лекарственных форм; (г) использование пролекарств (например, сулиндака). Однако, в силу того, что НПВС-гастродуоденопатия является не столько местной, сколько системной реакцией, эти подходы не решают проблему.
III. Применение селективных НПВС.
Как отмечалось выше, существует два изофермента циклооксигеназы, которые блокируются НПВС: ЦОГ-2, ответственный за продукцию простагландинов при воспалении, и ЦОГ-1, который контролирует выработку простагландинов, поддерживающих целостность слизистой желудочно-кишечного тракта, почечный кровоток и функцию тромбоцитов. Следовательно, селективные ингибиторы ЦОГ-2 должны вызывать меньше нежелательных реакций. Первыми такими препаратами являются мелоксикам и набуметон. Контролируемые исследования, проведенные у больных ревматоидным артритом и остеоартрозом, показали, что они переносятся лучше, чем диклофенак, пироксикам, ибупрофен и напроксен, не уступая им по эффективности (6).
Развитие язвы желудка у больного требует отмены НПВС и применения противоязвенных препаратов. Продолжение приема НПВС, например, при ревматоидном артрите, возможно только на фоне параллельного назначения мизопростола и регулярном эндоскопическом контроле.
На рис. 2 приведен алгоритм профилактики и лечения НПВС-гастродуоденопатии.
Почки
Нефротоксичность является второй по значимости группой нежелательных реакций НПВС. Выявлены два основных механизма отрицательного влияния НПВС на почки.
I. Путем блокады синтеза ПГ-Е2 и простациклина в почках НПВС вызывают сужение сосудов и ухудшение почечного кровотока. Это ведет к развитию ишемических изменений в почках, снижению клубочковой фильтрации и объема диуреза. В результате могут происходить нарушения водно-электролитного обмена: задержка воды, отеки, гипернатриемия, гиперкалиемия, рост уровня креатинина в сыворотке, повышение артериального давления.
Наиболее выраженным влиянием на почечный кровоток обладают индометацин и фенилбутазон.
II. НПВС могут оказывать прямое воздействие на паренхиму почек, вызывая интерстициальный нефрит (так называемая "анальгетическая нефропатия"). Наиболее опасным в этом отношении является фенацетин. Возможно серьезное поражение почек вплоть до развития тяжелой почечной недостаточности. Описано развитие острой почечной недостаточности при использовании НПВС как следствие острого аллергического интерстициалъного нефрита.
Факторы риска нефротоксичности: возраст старше 65 лет, цирроз печени, предшествующая почечная патология, снижение объема циркулирующей крови, длительный прием НПВС, сопутствующий прием диуретиков.
Гематотоксичность
Наиболее характерна для пиразолидинов и пиразолонов. Самые грозные осложнения при их применении – апластическая анемия и агранулоцитоз.
Коагулопатия
НПВС тормозят агрегацию тромбоцитов и оказывают умеренный антикоагулянтный эффект за счет торможения образования протромбина в печени. В результате могут развиваться кровотечения, чаще из желудочно-кишечного тракта.
Гепатотоксичность
Могут отмечаться изменения активности трансаминаз и других ферментов. В тяжелых случаях – желтуха, гепатит.
Реакции гиперчувствительности (аллергия)
Сыпи, отек Квинке, анафилактический шок, синдромы Лайелла и Стивенса-Джонсона, аллергический интерстициальный нефрит. Кожные проявления чаще отмечаются при использовании пиразолонов и пиразолидинов.
Бронхоспазм
Как правило, развивается у больных бронхиальной астмой и, чаще, при приеме аспирина. Его причинами могут быть аллергические механизмы, а также торможение синтеза ПГ-Е2, который является эндогенным бронходилататором.
Пролонгация беременности и замедление родов
Данный эффект связан с тем, что простагландины (ПГ-Е2 и ПГ-F2a) стимулируют миометрий.
МЕРЫ КОНТРОЛЯ ПРИ ДЛИТЕЛЬНОМ ПРИМЕНЕНИИ
Желудочно-кишечный тракт
Больные должны быть предупреждены о симптомах поражения желудочно-кишечного тракта. Каждые 1-3 месяца следует проводить анализ кала на скрытую кровь (табл. 4). По-возможности, периодически проводить фиброгастродуоденоскопию.
Ректальные свечи с НПВС целесообразно использовать у больных, перенесших операции на верхних отделах желудочно-кишечного тракта, и у пациентов, одновременно получающих несколько лекарственных средств. Они не должны применяться при воспалении прямой кишки или ануса и после недавно перенесенных аноректальных кровотечений.
Таблица 4. Лабораторный контроль при длительном назначении НПВС
| Вид исследования | Каждые 2-3 недели | Каждые 1-3 месяца |
|---|---|---|
| Клинический анализ крови | + | |
| Клинический анализ мочи | + | |
| Анализ кала на скрытую кровь | + | |
| Клиренс креатинина | + | |
| Функциональные пробы печени | + |
Почки
Необходимо следить за появлением отеков, измерять артериальное давление, особенно у больных гипертензией. Один раз в 3 недели проводится клинический анализ мочи. Каждые 1-3 месяца необходимо определять уровень креатинина сыворотки и рассчитывать его клиренс.
Печень
При длительном назначении НПВС необходимо своевременно выявлять клинические признаки поражения печени. Каждые 1-3 месяца следует контролировать функцию печени, определять активность трансаминаз.
Кроветворение
Наряду с клиническим наблюдением следует один раз в 2-3 недели проводить клинический анализ крови. Особый контроль необходим при назначении производных пиразолона и пиразолидина (табл. 8).
ПРАВИЛА НАЗНАЧЕНИЯ И ДОЗИРОВАНИЯ
Индивидуализация выбора препарата
Для каждого больного следует подбирать наиболее эффективный препарат с наилучшей переносимостью. Причем, это может быть любое НПВС, но в качестве противовоспалительного необходимо назначать препарат из I группы. Чувствительность больных к НПВС даже одной химической группы может варьировать в широких пределах, поэтому неэффективность одного из препаратов еще не говорит о неэффективности группы в целом.
При использовании НПВС в ревматологии, особенно при замене одного препарата другим, необходимо учитывать, что развитие противовоспалительного эффекта отстает по времени от анальгезирующего. Последний отмечается в первые часы, в то время как противовоспалительный – через 10-14 дней регулярного приема, а при назначении напроксена или оксикамов еще позднее – на 2-4 неделе.
Дозировка
Любой новый для данного больного препарат необходимо назначать сначала в наименьшей дозе. При хорошей переносимости через 2-3 дня суточную дозу повышают. Терапевтические дозы НПВС находятся в широком диапазоне, причем в последние годы наметилась тенденция к увеличению разовых и суточных доз препаратов, характеризующихся наиболее хорошей переносимостью (напроксен, ибупрофен), при сохранении ограничений на максимальные дозы аспирина, индометацина, фенилбутазона, пироксикама. У некоторых больных лечебный эффект достигается только при использовании очень высоких доз НПВС.
Время приема
При длительном курсовом назначении (например, в ревматологии) НПВС принимают после еды. Но для получения быстрого анальгезирующего или жаропонижающего эффекта предпочтительнее назначать их за 30 минут до или через 2 часа после еды, запивая 1/2-1 стаканом воды. После приема в течение 15 минут желательно не ложиться в целях профилактики развития эзофагита.
Момент приема НПВС может определяться также временем максимальной выраженности симптомов заболевания (боль, скованность в суставах), то есть с учетом хронофармакологии препаратов. При этом можно отходить от общепринятых схем (2-3 раза в день) и назначать НПВС в любое время суток, что нередко позволяет достичь большего лечебного эффекта при меньшей суточной дозе.
При выраженной утренней скованности целесообразен как можно более ранний (сразу после пробуждения) прием быстро всасывающихся НПВС или назначение длительно действующих препаратов на ночь. Наибольшей быстротой всасывания в желудочнокишечном тракте и, следовательно, более быстрым наступлением эффекта обладают напроксен-натрий, диклофенак-калий, водорастворимый ("шипучий") аспирин, кетопрофен.
Монотерапия
Одновременное применение двух или более НПВС не целесообразно по следующим причинам:
– эффективность таких комбинаций объективно не доказана;
– в ряде подобных случаев отмечается снижение концентрации препаратов в крови (например, аспирин снижает концентрацию индометацина, диклофенака, ибупрофена, напроксена, пироксикама), что ведет к ослаблению эффекта;
– возрастает опасность развития нежелательных реакций. Исключением является возможность применения парацетамола в сочетании с каким-либо другим НПВС для усиления анальгезирующего эффекта.
У некоторых больных два НПВС могут назначаться в разное время суток, например, быстровсасывающийся – утром и днем, а длительнодействующий – вечером.
ЛЕКАРСТВЕННЫЕ ВЗАИМОДЕЙСТВИЯ
Довольно часто больным, которые получают НПВС, назначают и другие лекарственные препараты. При этом обязательно следует учитывать возможность их взаимодействия друг с другом. Так, НПВС могут усиливать действие непрямых антикоагулянтов и пероральных гипогликемических средств. В то же время, они ослабляют эффект антигипертензивных препаратов, повышают токсичность антибиотиков-аминогликозидов, дигоксина и некоторых других лекарственных средств, что имеет существенное клиническое значение и влечет за собой ряд практических рекомендаций (табл. 5). Следует, по-возможности, избегать одновременного назначения НПВС и диуретиков, ввиду, с одной стороны, ослабления диуретического эффекта и, с другой, риска развития почечной недостаточности. Наиболее опасной является комбинация индометацина с триамтереном.
Многие препараты, назначаемые одновременно с НПВС, в свою очередь, могут влиять на их фармакокинетику и фармакодинамику:
– алюминийсодержащие антациды (альмагель, маалокс и другие) и холестирамин ослабляют всасывание НПВС в желудочно-кишечном тракте. Поэтому сопутствующее назначение таких антацидов может потребовать увеличения дозы НПВС, а между приемами холестирамина и НПВС необходимы интервалы не менее 4 часов;
– натрия бикарбонат усиливает всасывание НПВС в желудочно-кишечном тракте;
– противовоспалительное действие НПВС усиливают глюкокортикоиды и "медленно действующие" (базисные) противовоспалительные средства (препараты золота, аминохинолины);
– анальгезирующий эффект НПВС усиливают наркотические анальгетики и седативные препараты.
БЕЗРЕЦЕПТУРНОЕ ПРИМЕНЕНИЕ НПВС
Для безрецептурного применения в течение многих лет в мировой практике широко применяются аспирин, парацетамол, метамизол, пропифеназон и их комбинации. В последние годы для безрецептурного использования разрешены ибупрофен, напроксен, напроксен-натрий и кетопрофен.
Таблица 5. Влияние НПВС на эффект других препаратов.
По Brooks P.M., Day R.O. 1991 (7) с дополнениями
| Препарат | НПВС | Действие | Рекомендации |
|---|---|---|---|
| Фармакокинетическое взаимодействие | |||
| Непрямые антикоагулянты | Фенилбутазон Оксифенбутазон | Торможение метаболизма в печени, усиление антикоагулянтного эффекта | Избегать этих НПВС, если возможно, или проводить строгий контроль |
| Все, особенно аспирин | Вытеснение из связи с белками плазмы, усиление антикоагулянтного эффекта | Избегать НПВС, если возможно, или проводить строгий контроль | |
| Пероральные гипогликемические препараты (производные сульфонилмочевины) | Фенилбутазон Оксифенбутазон | Торможение метаболизма в печени, усиление гипогликемического эффекта | Избегать НПВС, если возможно, или строго контролировать уровень глюкозы в крови |
| Все, особенно аспирин | Вытеснение из связи белками плазмы, усиление гипогликемического эффекта | ||
| Дигоксин | Все | Торможение почечной экскреции дигоксина при нарушении функции почек (особенно у детей младшего возраста и пожилых), повышение его концентрации в крови, увеличение токсичности. При нормальной функции почек взаимодействие менее вероятно | Избегать НПВС, если возможно, или строго контролировать клиренс креатининаи концентрацию дигоксина в крови |
| Антибиотики – аминогликозиды | Все | Торможение почечной экскреции аминогликозидов, повышение их концентрации в крови | Строгий контроль концентрации аминогликозидов в крови |
| Метотрексат (высокие "неревматологические" дозы) | Все | Торможение почечной экскреции метотрексата, повышение его концентрации в крови и токсичности (взаимодействие с "ревматологической" дозой метотрексата не отмечается) | Одновременное назначение противопоказано. Допустимо использование НПВС в промежутках химиотерапии |
| Препараты лития | Все (в меньшей степени – аспирин, сулиндак) | Торможение почечной экскреции лития, повышение его концентрации в крови и токсичности | Использовать аспирин или сулиндак, если необходимо назначение НПВС. Строгий контроль концентрации лития в крови |
| Фенитоин | Фенилбутазон Оксифенбутазон | Торможение метаболизма, повышение концентрации в крови и токсичности | Избегать этих НПВС, если возможно, или строго контролировать концентрацию фенитоина в крови |
| Фармакодинамическое взаимодействие | |||
| Антигипертензивные препараты Бета-блокаторы Диуретики Ингибиторы АПФ* | В наибольшей степени – индометацин, фенилбутазон. В наименьшей – сулиндак | Ослабление гипотензивного действия за счёт торможения синтеза ПГ в почках (задержка натрия и воды) и сосудах (вазоконстрикция) | Использовать сулиндак и, по-возможности, избегать других НПВС при гипертензии. Строгий контроль артериального давления. Может потребоваться усиление антигипертензивной терапии |
| Диуретики | В наибольшей степени – индометацин, фенилбутазон. В наименьшей – сулиндак | Ослабление диуретического и натрийуретического действия, ухудшение состояния при сердечной недостаточности | Избегать НПВС (кроме сулиндака) при сердечной недостаточности, строго контролировать состояние пациента |
| Непрямые антикоагулянты | Все | Увеличение риска желудосно-кишечных кровотечений вследствие повреждения слизистой и торможения агрегации тромбоцитов | Избегать НПВС, если возможно |
| Комбинации повышенного риска | |||
| Диуретики Все | Все (в меньшей степени – сулиндак) | Повышенный риск развития почечной недостаточности | Комбинация противопоказана |
| Триамтерен | Индометацин | Высокий риск развития острой почечной недостаточности | Комбинация противопоказана |
| Все калийсберегающие | Все | Высокий риск развития гиперкалиемии | Избегать таких комбинаций или строго контролировать уровень калия в плазме |
Показания: для оказания анальгезирующего и жаропонижающего действия при простудных заболеваниях, головной и зубной боли, мышечных и суставных болях, болях в спине, дисменорее.
Необходимо предупреждать больных о том, что НПВС оказывают только симптоматическое действие и не обладают ни антибактериальной, ни противовирусной активностью. Поэтому при сохранении лихорадки, боли, ухудшения общего состояния они должны обращаться к врачу.
ХАРАКТЕРИСТИКА ОТДЕЛЬНЫХ ПРЕПАРАТОВ
НПВС С ВЫРАЖЕННОЙ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ
НПВС, относящиеся к данной группе, обладают клинически значимым противовоспалительным действием, поэтому находят широкое применение прежде всего в качестве противовоспалительных средств, в том числе при ревматологических заболеваниях у взрослых и детей. Многие из препаратов используются также как анальгетики и антипиретики.
АЦЕТИЛСАЛИЦИЛОВАЯ КИСЛОТА
(Аспирин, Аспро, Колфарит)
Ацетилсалициловая кислота является старейшим НПВС. При проведении клинических испытаний она, как правило, служит стандартом, с эффективностью и переносимостью которого сравнивают другие НПВС.
Аспирин – это торговое название ацетилсалициловой кислоты, предложенное фирмой "Байер" (Германия). С течением времени оно стало настолько отождествляться с данным препаратом, что сейчас в большинстве стран мира используется как генерическое.
Фармакодинамика
Фармакодинамика аспирина зависит от суточной дозы:
малые дозы – 30-325 мг – вызывают торможение агрегации тромбоцитов;
средние дозы – 1,5-2 г – оказывают анальгезирующее и жаропонижающее действие;
большие дозы – 4-6 г – обладают противовоспалительным эффектом.
В дозе более 4 г аспирин усиливает экскрецию мочевой кислоты (урикозурическое действие), при назначении в меньших дозах ее выведение задерживается.
Фармакокинетика
Хорошо всасывается в желудочно-кишечном тракте. Всасывание аспирина усиливается при измельчении таблетки и приеме ее с теплой водой, а также при использовании "шипучих" таблеток, которые перед приемом растворяются в воде. Период полувыведения аспирина составляет всего 15 минут. Под действием эстераз слизистой желудка, печени и крови от аспирина отщепляется салицилат, который обладает основной фармакологической активностью. Максимальная концентрация салицилата в крови развивается через 2 часа после приема аспирина, период полувыведения его составляет 4-6 часов. Метаболизируется в печени, выделяется с мочой, причем при повышении рН мочи (например, в случае назначения антацидов) выведение усиливается. При использовании больших доз аспирина возможно насыщение метаболизирующих ферментов и увеличение периода полувыведения салицилата до 15-30 часов.
Взаимодействия
Глюкокортикоиды ускоряют метаболизм и экскрецию аспирина.
Всасывание аспирина в желудочно-кишечном тракте усиливают кофеин и метоклопрамид.
Аспирин ингибирует желудочную алкоголь-дегидрогеназу, что ведет к повышению уровня этанола в организме, даже при его умеренном (0,15 г/кг) употреблении (8).
Нежелательные реакции
Гастротоксичностпъ. Даже при использовании в низких дозах – 75-300 мг/сут (в качестве антиагреганта) – аспирин может вызывать повреждение слизистой желудка и вести к развитию эрозий и/или язв, которые довольно часто осложняются кровотечениями. Риск кровотечений является дозозависимым: при назначении в дозе 75 мг/сут он на 40% ниже, чем в дозе 300 мг, и на 30% ниже, чем в дозе 150 мг (9). Даже незначительно, но постоянно кровоточащие эрозии и язвы могут вести к систематической потере крови с калом (2-5 мл/сут) и развитию железодефицитной анемии.
Несколько меньшую гастротоксичность имеют лекарственные формы с кишечно-растворимым покрытием. У некоторых больных, принимающих аспирин, возможно развитие адаптации к его гастротоксическому действию. В ее основе лежит местное усиление митотической активности, уменьшение нейтрофильной инфильтрации и улучшение кровотока (9).
Повышенная кровоточивость вследствие нарушения агрегации тромбоцитов и торможения синтеза протромбина в печени (последнее – при дозе аспирина более 5 г/сут), поэтому применение аспирина в сочетании с антикоагулянтами опасно.
Реакции гиперчувствительности: кожные сыпи, бронхоспазм. Выделяется особая нозологическая форма – синдром Фернан-Видаля ("аспириновая триада"): сочетание полипоза носа и/или придаточных пазух, бронхиальной астмы и полной непереносимости аспирина. Поэтому аспирин и другие НПВС рекомендуется с большой осторожностью применять у больных бронхиальной астмой.
Синдром Рея – развивается при назначении аспирина детям с вирусными инфекциями (грипп, ветряная оспа). Проявляется тяжелой энцефалопатией, отеком мозга и поражением печени, которое протекает без желтухи, но с высоким уровнем холестерина и печеночных ферментов. Дает очень высокую летальность (до 80%). Поэтому не следует применять аспирин при острых респираторных вирусных инфекциях у детей первых 12 лет жизни.
Передозировка или отравление в легких случаях проявляется симптомами "салицилизма": шум в ушах (признак "насыщения" салицилатом), оглушенность, снижение слуха, головная боль, нарушения зрения, иногда тошнота и рвота. При тяжелой интоксикации развиваются нарушения со стороны центральной нервной системы и водно-электролитного обмена. Отмечается одышка (как результат стимуляции дыхательного центра), нарушения кислотно-основного состояния (сначала респираторный алкалоз из-за потерь углекислоты, затем метаболический ацидоз вследствие угнетения тканевого обмена), полиурия, гипертермия, обезвоживание. Возрастает потребление кислорода миокардом, может развиться сердечная недостаточность, отек легких. Наиболее чувствительны к токсическому действию салицилата дети до 5 лет, у которых так же, как и у взрослых, оно проявляется выраженными нарушениями кислотно-основного состояния и неврологическими симптомами. Тяжесть интоксикации зависит от принятой дозы аспирина (табл. 6).
При приеме 150-300 мг/кг отмечается интоксикация от слабой до умеренной степени, доза 300-500 мг/кг ведет к тяжелому отравлению, а доза более 500 мг/кг является потенциально летальной. Меры помощи приведены в табл. 7.
Таблица 6. Симптомы острого отравления аспирином у детей. (Applied Therapeutics, 1996) [10]
| Принятая доза (мг/кг) | Степень интоксикации | Симптоматика |
|---|---|---|
| 150-300 | Слабая/умеренная | Слабая: одышка от слабой до умеренной степени, иногда заторможенность. Умеренная: сильная одышка, заторможенность или возбуждение |
| 300-500 | Тяжёлая | Сильная одышка, кома, иногда судороги |
| > 500 | Потенциально летальная | Кома, судороги, коллапс |
Таблица 7. Меры помощи при интоксикации аспирином.
- Промывание желудка
- Введение активированного угля – до 15 г
- Обильное питье (молоко, сок) – до 50-100 мл/кг/сутки
- Внутривенное введение полиионных гипотонических растворов (1 часть 0,9% натрия хлорида и 2 части 10% глюкозы)
- При коллапсе – внутривенное введение коллоидных растворов
- При ацидозе – внутривенное введение натрия бикарбоната. Не рекомендуется вводить до определения рН крови, особенно у детей, при анурии
- Внутривенное введение калия хлорида
- Физическое охлаждение с помощью воды, но не спирта!
- Гемосорбция
- Заменное переливание крови
- При почечной недостаточности – гемодиализ
Показания
Аспирин является одним из препаратов выбора для лечения ревматоидного артрита, в том числе и ювенильного. Согласно рекомендациям большинства последних руководств по ревматологии противовоспалительную терапию при ревматоидном артрите следует начинать именно с аспирина. При этом, однако, необходимо иметь в виду, что его противовоспалительный эффект проявляется при приеме высоких доз, которые могут плохо переноситься многими больными.
Очень часто аспирин используется как анальгетик и антипиретик. Контролируемые клинические исследования показали, что аспирин может оказывать эффект при многих болях, включая болевой синдром при злокачественных опухолях (11). Сравнительная характеристика анальгезирующего действия аспирина и других НПВС представлена в табл. 8.
Несмотря на то, что большинство НПВС in vitro обладает способностью тормозить агрегацию тромбоцитов, в клинике в качестве антиагреганта наиболее широко применяется аспирин, так как в контролируемых клинических исследованиях доказана его эффективность при стенокардии, инфаркте миокарда, транзиторных нарушениях мозгового кровообращения и некоторых других заболеваний. Аспирин назначают сразу же при подозрении на инфаркт миокарда или ишемический инсульт. В то же время, аспирин слабо влияет на тромбообразование в венах, поэтому его не следует использовать для профилактики послеоперационных тромбозов в хирургии, где препаратом выбора является гепарин.
Установлено, что при длительном систематическом (многолетнем) приеме в малых дозах (325 мг/сут) аспирин снижает частоту развития колоректального рака. В первую очередь профилактический прием аспирина показан лицам из групп риска по колоректальному раку: семейный анамнез (колоректальный рак, аденома, аденоматозный полипоз); воспалительные заболевания толстого кишечника; рак груди, яичников, эндометрия; рак или аденома толстого кишечника (12).
Таблица 8. Сравнительная характеристика анальгезирующего действия аспирина и других НПВС.
Drugs of Choice from the Medical Letter, 1995 [11]
| Препарат | Разовая доза | Интервал | Максимальная суточная доза | Примечание |
|---|---|---|---|---|
| Аспирин | Внутрь 500-1000 мг | 4-6 часов | 4000 мг | Продолжительность действия после однократного приема 4 часа |
| Парацетамол | Внутрь 500-1000 мг | 4-6 часов | 4000 мг | По эффективности равен аспирину; 1000 мг обычно эффективнее, чем 650 мг; продолжительность действия 4 часа. |
| Дифлунизал | Внутрь 1-я доза 1000 мг, далее по 500 мг | 8-12 часов | 1500 мг | 500 мг дифлунизала > 650 мг аспирина или парацетамола, примерно равны комбинации парацетамол/кодеин; действует медленно, но продолжительно |
| Диклофенак-калий | Внутрь 50 мг | 8 часов | 150 мг | Сравним с аспирином, более длительное действие |
| Этодолак | Внутрь 200-400 мг | 6-8 часов | 1200 мг | 200 мг примерно равны 650 мг аспирина, 400 мг > 650 мг аспирина |
| Фенопрофен | Внутрь 200 мг | 4-6 часов | 1200 мг | Сравним с аспирином |
| Флурбипрофен | Внутрь 50-100 мг | 6-8 часов | 300 мг | 50 мг > 650 мг аспирина; 100 мг > комбинации парацетамол/кодеин |
| Ибупрофен | Внутрь 200-400 мг | 4-8 часов | 2400 мг | 200 мг = 650 мг аспирина или парацетамола; 400 мг = комбинации парацетамол/кодеин |
| Кетопрофен | Внутрь 25-75 мг | 4-8 часов | 300 мг | 25 мг = 400 мг ибупрофена и > 650 мг аспирина; 50 мг > комбинации парацетамол/кодеин |
| Кеторолак | Внутримышечно 30-60 мг | 6 часов | 120 мг | Сравним с 12 мг морфина, более длительное действие, курс не более 5 дней |
| Мефенамовая кислота | Внутрь 1-я доза 500 мг, далее 250 мг | 6 часов | 1250 мг | Сравнима с аспирином, но более эффективна при дисменорее, курс не более 7 дней |
| Напроксен | Внутрь 1-я доза 500 мг, далее по 250 мг | 6-12 часов | 1250 мг | 250 мг примерно равны 650 мг аспирина, более медленное, но длительное действие; 500 мг > 650 мг аспирина, быстрота эффекта такая же, как у аспирина |
| Напроксен-натрий | Внутрь 1-я доза 550 мг, далее по 275 мг | 6-12 часов | 1375 мг | 275 мг примерно равны 650 мг аспирина, более медленное, но длительное действие; 550 мг > 650 мг аспирина, быстрота эффекта макая же, как у аспирина |
Дозировка
Взрослые: неревматические заболевания – 0,5 г 3-4 раза в день; ревматические заболевания – начальная доза – 0,5 г 4 раза в день, затем ее увеличивают на 0,25-0,5 г в день каждую неделю;
как антиагрегант – 100-325 мг/день в один прием.
Дети: неревматические заболевания – в возрасте до 1 года – 10 мг/кг 4 раза в день, старше года – 10-15 мг/кг 4 раза в день;
ревматические заболевания – при массе тела до 25 кг – 80-100 мг/кг/день, при массе более 25 кг – 60-80 мг/кг/день.
Формы выпуска:
– таблетки по 100, 250, 300 и 500 мг;
– "шипучие таблетки" АСПРО-500. Входит в состав комбинированных препаратов алказельтцер, аспирин С, аспро-С форте, цитрамон П и других.
ЛИЗИНМОНОАЦЕТИЛСАЛИЦИЛАТ
(Аспизол, Ласпал)
Производное аспирина для парентерального введения. Превосходит его по быстроте и силе анальгезирующего эффекта. Нежелательные реакции такие же, как у аспирина.
Показания
Купирование острого болевого синдрома (ревматические боли, радикулит, послеоперационные и посттравматические боли, колики); кроме того, используется при гипертермии, тромбофлебите.
Дозировка
Взрослые: разовая доза – 2 г, максимально – до 10 г/сутки.
Дети: 20-50 мг/кг в день в 2-3 введения.
Форма выпуска:
– флаконы по 1 г (соответствует 500 мг аспирина) с растворителем (5 мл воды для инъекций).
ДИФЛУНИЗАЛ (Долобид)
Относится к группе неацетилированных салицилатов. Не метаболизируется до салицилата и поэтому не вызывает явлений салицилизма. Обладает мощным противовоспалительным и, особенно, анальгезирующим эффектами, проявляет урикозурическое действие. В отличие от аспирина дифлунизал не обладает жаропонижающим действием, так как не проникает в центральную нервную систему. Он тормозит агрегацию тромбоцитов только при назначении максимальных доз (2 г/день), и этот эффект обратим.
Фармакокинетика
Хорошо всасывается в желудочно-кишечном тракте. Максимальная концентрация в крови развивается через 2-3 часа, но анальгезирующий эффект отмечается уже в 1-й час после приема, особенно в ударной дозе (1000 мг). Имеет более длительный, чем аспирин, период полувыведения – 8-12 часов.
Нежелательные реакции
Подобны аспирину, однако гастротоксичность ниже, а развитие синдрома Рея не описано.
Показания
Ревматоидный артрит, остеоартроз, болевой синдром (включая дисменорею).
Дозировка
Взрослые: при ревматоидном артрите и остеоартрозе по 0,5-1 г каждые 12 часов; для купирования боли (в том числе при дисменорее): 1-я доза – 1 г, затем по 0,5 г каждые 8-12 часов.
Детям не назначается.
Форма выпуска:
– таблетки по 500 мг.
ФЕНИЛБУТАЗОН (Бутадион)
Превосходит аспирин по силе противовоспалительного эффекта. Усиливает выведение из организма мочевой кислоты.
Фармакокинетика
Максимальная концентрация в крови развивается через 2 часа после приема внутрь и только через 6-8 часов после введения внутримышечно (так как фенилбутазон связывается тканями в месте инъекции). Период полувыведения составляет около 70 часов. Один из метаболитов фенилбутазона – оксифенбутазон – выпускается в виде отдельного препарата и по всем параметрам (включая токсичность) равноценен фенилбутазону.
Взаимодействия
Фенилбутазон является одним из наиболее сильных "вытеснителей" других лекарственных средств из связи с альбуминами плазмы, что ведет к повышению концентрации свободной (активной) фракции этих лекарственных средств в крови. Кроме того, он может угнетать метаболизм некоторых препаратов в печени. Поэтому, при сочетании с фенилбутазоном возможно усиление действия непрямых антикоагулянтов, оральных противодиабетических препаратов, сульфаниламидов и других лекарственных средств.
Ухудшая почечный кровоток, фенилбутазон ослабляет действие диуретиков и антигипертензивных препаратов (табл. 5).
Нежелательные реакции
Широкое использование фенилбутазона ограничивают его частые и серьезные нежелательные реакции, которые встречаются у 45% больных. Наиболее опасно депрессивное действие препарата на костный мозг, следствием которого являются гематотоксические реакции – апластическая анемия и агранулоцитоз, часто вызывающие летальный исход. Риск апластической анемии более высок у женщин, у людей старше 40 лет, при длительном применении. Однако и при кратковременном приеме лицами молодого возраста может развиться фатальная апластическая анемия. Отмечаются также лейкопения, тромбоцитопения, панцитопения и гемолитическая анемия.
Кроме того, отмечаются нежелательные реакции со стороны желудочно-кишечного тракта (эрозивно-язвенные поражения, кровотечения, диарея), задержка жидкости в организме с появлением отеков, кожные сыпи, язвенный стоматит, увеличение слюнных желез, расстройства центральной нервной системы (заторможенность, возбуждение, тремор), гематурия, протеинурия, поражения печени.
Фенилбутазон обладает кардиотоксичностью (у больных с сердечной недостаточностью возможно ее обострение) и может вызывать острый легочный синдром, проявляющийся одышкой и лихорадкой. У ряда пациентов наблюдаются реакции гиперчувст-вительности в виде бронхоспазма, генерализованной лимфаденопатии, кожных сыпей, синдромов Лайелла и Стивенса-Джонсона. Фенилбутазон и особенно его метаболит оксифенбутазон могут вести к обострению порфирии.
Показания
Фенилбутазон следует использовать как резервное НПВС при неэффективности других препаратов, коротким курсом. Наибольший эффект отмечается при болезни Бехтерева, подагре.
Предупреждения
Нельзя применять фенилбутазон и содержащие его комбинированные препараты (реопирит, пирабутол) как анальгетики или антипиретики в широкой клинической практике.
Учитывая возможность развития опасных для жизни гематологических осложнений, необходимо предупреждать больных об их ранних проявлениях и строго соблюдать правила назначения пиразолонов и пиразолидинов (табл. 9).
Таблица 9. Правила применения фенилбутазона и других производных пиразолидина и пиразолона
- Назначать только после тщательного сбора анамнеза, клинического и лабораторного обследования с определением эритроцитов, лейкоцитов и тромбоцитов. Эти исследования должны быть повторены при малейшем подозрении на гематотоксичность.
- Пациентов необходимо предупреждать о немедленном прекращении лечения и срочном обращении к врачу при появлении следующих симптомов:
- лихорадка, озноб, боль в горле, стоматит (симптомы агранулоцитоза);
- диспепсия, боли в эпигастрии, необычные кровотечения и кровоподтеки, дегтеобразный стул (симптомы анемии);
- кожная сыпь, зуд;
- значительная прибавка массы тела, отеки.
- Для оценки эффективности достаточно недельного курса. При отсутствии эффекта препарат должен быть отменен. У больных старше 60 лет фенилбутазон не должен применяться более 1 недели.
Фенилбутазон противопоказан больным с нарушениями кроветворения, эрозивно-язвенными поражениями желудочно-кишечного тракта (включая наличие их в анамнезе), сердечно-сосудистыми заболеваниями, патологией щитовидной железы, нарушениями функции печени и почек, при аллергии к аспирину и другим НПВС. Он может ухудшать состояние больных системной красной волчанкой.
Дозировка
Взрослые: начальная доза – 450-600 мг/день в 3-4 приема. После достижения терапевтического эффекта используются под-держивающие дозы – 150-300 мг/день в 1-2 приема.
У детей до 14 лет не применяется.
Формы выпуска:
– таблетки по 150 мг;
– мазь, 5%.
КЛОФЕЗОН (Перклюзон)
Эквимолярное соединение фенилбутазона и клофексамида. Клофексамид обладает преимущественно анальгезирующим и меньшим противовоспалительным действием, дополняя эффект фенилбутазона. Переносимость клофезона несколько лучше, чем фенилбутазона. Нежелательные реакции развиваются реже, но необходимо соблюдать меры предосторожности (табл. 7).
Показания к применению
Показания к применению такие же, как у фенилбутазона
Дозировка
Взрослые: по 200-400 мг 2-3 раза в день внутрь или ректально.
Дети с массой тела более 20 кг: 10-15 мг/кг/день.
Формы выпуска:
– капсулы по 200 мг;
– свечи по 400 мг;
– мазь (1 г содержит 50 мг клофезона и 30 мг клофексамида).
ИНДОМЕТАЦИН
(Индоцид, Индобене, Метиндол, Эльметацин)
Индометацин является одним из наиболее мощных НПВС.
Фармакокинетика
Максимальная концентрация в крови развивается через 1-2 часа после приема внутрь обычных и через 2-4 часа после приема пролонгированных ("ретард") лекарственных форм. Прием пищи замедляет всасывание. При ректальном введении всасывается несколько хуже и максимальная концентрация в крови развивается медленнее. Период полувыведения составляет 4-5 часов.
Взаимодействия
Индометацин больше, чем другие НПВС, ухудшает почечный кровоток, поэтому может значительно ослаблять действие диуретиков и антигипертензивных средств. Сочетание индометацина с калийсберегающим диуретиком триамтереном очень опасно, так как провоцирует развитие острой почечной недостаточности.
Нежелательные реакции
Главный недостаток индометацина – частое развитие нежелательных реакций (у 35-50% больных), причем их частота и выраженность зависят от суточной дозы. В 20% случаев из-за нежелательных реакций препарат отменяют.
Наиболее характерны нейротоксические реакции: головная боль (вызванная отеком мозга), головокружение, оглушенность, торможение рефлекторной деятельности; гастротоксичность (выше, чем у аспирина); нефротоксичность (не следует использовать при почечной и сердечной недостаточности); реакции гиперчувствительности (возможна перекрестная аллергия с аспирином).
Показания
Индометацин особенно эффективен при анкилозирующем спондилите и остром приступе подагры. Широко используется при ревматоидном артрите и активном ревматизме. При ювенильном ревматоидном артрите является препаратом резерва. Имеется большой опыт применения индометацина при остеоартрозах тазобедренного и коленного суставов. Однако недавно было показано, что у больных остеоартрозами он ускоряет деструкцию суставного хряща. Особой областью использования индометацина является неонаталогия (см. ниже).
Предупреждения
За счет мощного противовоспалительного эффекта индометацин может маскировать клинические симптомы инфекций, по-этому у больных с инфекциями его применять не рекомендуется.
Дозировка
Взрослые: начальная доза – 25 мг 3 раза в день, максимально – 150 мг/день. Дозу увеличивают постепенно. Таблетки "ретард" и ректальные свечи назначают 1-2 раза в день. Иногда их применяют только на ночь, а утром и днем назначают другое НПВС. Наружно применяют мазь.
Дети: 2-3 мг/кг/день в 3 приема.
Формы выпуска:
– таблетки с кишечнорастворимым покрытием по 25 мг; – таблетки "ретард" по 75 мг; – свечи по 100 мг; – мазь, 5 и 10%.
Применение индометацина в неонатологии
Индометацин используется у недоношенных новорожденных для фармакологического закрытия открытого артериального протока. Причем, в 75-80% препарат позволяет добиться полного закрытия артериального протока и избежать оперативного вмешательства. Эффект индометацина обусловлен ингибированием синтеза ПГ-Е1, который поддерживает артериальный проток в открытом состоянии. Лучшие результаты отмечаются у детей с III-IV степенью недоношенности.
Показания к назначению индометацина для закрытия артериального протока:
- Масса тела при рождении до 1750 г.
- Выраженные нарушения гемодинамики – одышка, тахикардия, кардиомегалия.
- Неэффективность традиционной терапии, проведенной в течение 48 часов (ограничение жидкости, диуретики, сердечные гликозиды).
Противопоказания: инфекции, родовая травма, коагулопатии, патология почек, некротический энтероколит.
Нежелательные реакции: в основном, со стороны почек – ухудшение кровотока, повышение креатинина и мочевины крови, снижение клубочковой фильтрации, диуреза.
Дозировка
Внутрь 0,2-0,3 мг/кг 2-3 раза каждые 12-24 часа. При отсутствии эффекта дальнейшее применение индометацина противопоказано.
СУЛИНДАК (Клинорил)
Фармакокинетика
Является "пролекарством", в печени превращается в активный метаболит. Максимальная концентрация активного метаболита сулиндака в крови отмечается через 3-4 часа после приема внутрь. Период полувыведения сулиндака – 7-8 часов, а активного метаболита – 16-18 часов, что обеспечивает продолжительный эффект и возможность приема 1-2 раза в день.
Нежелательные реакции
В отличие от индометацина менее гастро– и нейротоксичен, значительно слабее влияет на почечный кровоток и клубочковую фильтрацию (так как активный метаболит сулиндака не нарушает синтеза ПГ в почках), почти не взаимодействует с диуретиками и антигипертензивными препаратами. Может вызывать кристаллурию, поэтому не следует назначать больным мочекаменной болезнью. Гепатотоксичность выше, чем у индометацина.
Показания
Применяется при ревматических и неревматических заболеваниях.
Дозировка
Взрослые: внутрь 400 мг/день в 1-2 приема.
Дети: 4,5-6 мг/кг/день в 2 приема.
Форма выпуска:
– таблетки по 200 мг.
ЭТОДОЛАК (Эльдерин)
Фармакокинетика
Быстро и практически полностью всасывается в желудочно-кишечном тракте. Период полувыведения составляет 7 часов.
Нежелательные реакции
Переносится лучше, чем индометацин. Обладает более слабой гастротоксичностью благодаря меньшему ингибирующему влиянию на синтез ПГ-Е2 в слизистой желудка.
Показания
Ревматоидный артрит, болезнь Бехтерева, остеоартроз, болевой синдром различной локализации. Однократный прием препарата в дозе 200-400 мг обеспечивает послеоперационную анальгезию на 6-8 часов (3).
Дозировка
Взрослые: внутрь 200-400 мг каждые 6-8 часов. Максимальная суточная доза – 1200 мг. У детей не применяется.
Форма выпуска:
– таблетки по 200 и 300 мг.
ДИКЛОФЕНАК-НАТРИЙ
(Вольтарен, Диклобене, Диклонат П, Наклофен, Ортофен)
Является наиболее широко используемым НПВС в мире.
Фармакокинетика
Диклофенак хорошо всасывается в желудочно-кишечном тракте. Биодоступность составляет 50-60%, что обусловлено эффектом "первого прохождения". Максимальная концентрация в крови развивается через 0,5-2 часа после приема внутрь и через 10-30 минут после введения внутримышечно. Период полувыведения – 1,5-2 часа.
Нежелательные реакции
Диклофенак в целом хорошо переносится. Нежелательные реакции, как правило, развиваются реже, чем при использовании многих других НПВС. Но при длительном применении препарат может оказать отрицательное влияние на желудочно-кишечный тракт и, особенно, на печень, поэтому необходим клинический и лабораторный контроль.
Показания
Диклофенак сочетает высокую, на уровне индометацина, противовоспалительную активность с хорошей переносимостью при длительном приеме, широко используется в ревматологии.
Обладает сильным и быстрым анальгезирующим действием. При выраженном болевом синдроме (почечная или печеночная колика, послеоперационные боли, боли при травме) вводится внутримышечно.
Дозировка
Взрослые: по 25-50 мг 2-3 раза в день внутрь или ректально; таблетки "ретард" (по 100 мг) назначаются 1-2 раза в день. Внутримышечно по 75 мг 1-2 раза в день, при неэффективности первой дозы вторую можно ввести через 30 минут.
Дети старше 1,5 лет: 2-4 мг/кг/день в 2 приема внутрь или ректально.
Формы выпуска:
– таблетки с кишечнорастворимым покрытием по 25 мг; – таблетки "ретард" по 100 мг; – ампулы по 3 мл (25 мг/мл); – свечи по 25 и 50 мг; – гель, 1%.
ДИКЛОФЕНАК-КАЛИЙ (Вольтарен рапид)
По сравнению с диклофенак-натрием быстрее всасывается, причем, преимущественно, в желудке; оказывает более быстрый анальгезирующий эффект – через 20-30 минут после приема внутрь
Показания
Такие же, как у диклофенак-натрия. Показан для быстрого купирования болей.
Дозировка
Взрослые, внутрь 100-150 мг/день в 2-3 приема. При дисменорее суточная доза может быть увеличена до 200 мг.
Дети: дозы не установлены.
Форма выпуска:
– таблетки по 25 и 50 мг.
ПИРОКСИКАМ (Фельден, Пирокам, Эразон)
Обладает сильным противовоспалительным эффектом, который развивается медленно – в течение 1-2 недель постоянного приема. Максимальный эффект отмечается через 2-4 недели. Оказывает быстрое и выраженное анальгезирующее действие, особенно при внутримышечном введении.
Фармакокинетика
Хорошо всасывается в желудочно-кишечном тракте. Пища замедляет скорость всасывания. Максимальная концентрация в крови развивается через 3-5 часов. Имеет длительный период по-лувыведения – 45-60 часов. Равновесная концентрация в крови создается через 7-12 дней, поэтому клинический эффект развивается медленно. Более быстро равновесная концентрация достигается при приеме дозы насыщения.
Нежелательные реакции
Пироксикам является одним из наиболее гастротоксичных НПВС, особенно при длительном назначении в дозе 30 мг в сутки и выше. По некоторым данным, его гастротоксичность выше, чем у индометацина. Возможны и другие нежелательные реакции: гематотоксичность (тромбоцитопения, апластическая анемия, снижение уровня гемаглобина и гематокрита, не связанные с желудочно-кишечным кровотечением), нефротоксичность, кожные реакции (сыпи, фотодерматит).
Показания
Применяется как противовоспалительное средство, в том числе при ювенильном ревматоидном артрите, при подагре. Может использоваться как анальгетик при послеоперационных и пост-травматических болях.
Дозировка
Взрослые: 20 мг/день в один прием внутрь или ректально. Для быстрого эффекта в первые 2 дня назначают дозу насыщения – 40 мг/день в один или несколько приемов, а затем снижают до 20 мг/день. При остром приступе подагры в 1-й день – 40 мг в один прием, в последующие 4-6 дней – по 40 мг/день в один или несколько приемов.
Дети: при массе тела менее 15 кг – 5 мг/день, 16-25 кг – 10 мг/день, 26-45 кг – 15 мг/день, более 45 кг – 20 мг/день.
Формы выпуска:
– таблетки и капсулы по 10 и 20 мг;
– ампулы по 1 и 2 мл (20 мг/мл);
– гель, 0,5%.
ТЕНОКСИКАМ (Тилкотил)
По активности и фармакокинетическим параметрам близок к пироксикаму. Максимальная концентрация в крови развивается через 1-2,6 часа при приеме натощак и через 4-6 часов при приеме после еды. Период полувыведения составляет 60-75 часов. Полный клинический эффект развивается через 2 недели. Менее гастротоксичен, чем пироксикам.
Дозировка
Взрослые: внутрь, ректально и внутримышечно – 20 мг/сутки в один прием (введение).
Дети: дозы не установлены.
Формы выпуска:
– таблетки по 20 мг;
– капсулы по 20 мг;
– свечи по 20 мг.
ЛОРНОКСИКАМ (Ксефокам)
НПВС из группы оксикамов – хлортеноксикам. По ингибированию ЦОГ превосходит другие оксикамы, причем примерно в одинаковой степени блокирует ЦОГ-1 и ЦОГ-2, занимая промежуточное положение в классификации НПВС, построенной по принципу селективности. Обладает выраженным анальгезирующим и противовоспалительным действием.
Анальгезирующий эффект лорноксикама складывается из нарушения генерации болевых импульсов и ослабления восприятия боли (особенно при хронических болях). При в/в введении препарат способен повышать уровень эндогенных опиоидов, активируя тем самым физиологическую антиноцицептивную систему организма.
Фармакокинетика
Хорошо всасывается в ЖКТ, пища несколько снижает биодоступность. Максимальные концентрации в плазме крови отмечаются через 1-2 ч. При в/м введении максимальный уровень в плазме отмечается через 15 мин. Хорошо проникает в синовиальную жидкость, где его концентрации достигают 50% плазменных, и длительно в ней сохраняется (до 10-12 ч). Метаболизируется в печени, выводится через кишечник (преимущественно) и почки. Период полувыведения – 3-5 ч.
Нежелательные реакции
Лорноксикам менее гастротоксичен, чем оксикамы "первого поколения" (пироксикам, теноксикам). Отчасти это связано с коротким периодом полувыведения, благодаря которому создаются возможности для восстановления протекторного уровня ПГ в слизистой оболочке ЖКТ. В контролируемых исследованиях выявлено, что лорноксикам по переносимости превосходит индометацин и практически не уступает диклофенаку.
Показания
– Болевой синдром (острые и хронических боли, включая онкологические).
При в/в введении лорноксикам в дозе 8 мг не уступает по выраженности обезболивающего эффекта меперидину (близок отечественному промедолу). При пероральном приеме у пациентов с послеоперационными болями 8 мг лорноксикама примерно равноценны 10 мг кеторолака, 400 мг ибупрофена и 650 мг аспирина. При тяжелом болевом синдроме лорноксикам может применяться в сочетании с опиоидными анальгетиками, что позволяет снизить дозу последних.
– Ревматические заболевания (ревматоидный артрит, псориатический артрит, остеоартроз).
Дозировка
Взрослые:
при болевом синдроме – внутрь – 8 мг х 2 раза в день; возможен прием ударной дозы 16 мг; в/м или в/в – 8-16 мг (1-2 дозы с интервалом 8-12 часов); в ревматологии – внутрь 4-8 мг х 2 раза в день.
Дозы для детей до 18 лет не установлены.
Формы выпуска:
– таблетки по 4 и 8 мг;
– флаконы по 8 мг (для приготовления инъекционного раствора).
МЕЛОКСИКАМ (Мовалис)
Является представителем нового поколения НПВС – селективных ингибиторов ЦОГ-2. Благодаря этому свойству мелоксикам избирательно тормозит образование простагландинов, участвующих в формировании воспаления. В то же время, он значительно слабее ингибирует ЦОГ-1, поэтому меньше влияет на синтез простагландинов, регулирующих почечный кровоток, выработку защитной слизи в желудке и агрегацию тромбоцитов.
Контролируемые исследования, проведенные у больных ревматоидным артритом, показали, что по силе противовоспалительной активности мелоксикам не уступает пироксикаму, напроксену и диклофенаку, но достоверно меньше вызывает нежелательные реакции со стороны желудочно-кишечного тракта и почек (13).
Фармакокинетика
Биодоступность при приеме внутрь составляет 89% и не зависит от приема пищи. Максимальная концентрация в крови развивается через 5-6 часов. Равновесная концентрация создается через 3-5 дней. Период полувыведения 20 часов, что позволяет назначать препарат 1 раз в сутки.
Показания
Ревматоидный артрит, остеоартроз.
Дозировка
Взрослые: внутрь и внутримышечно по 7,5-15 мг 1 раз в сутки.
У детей эффективность и безопасность препарата не изучена.
Формы выпуска:
– таблетки по 7,5 и 15 мг;
– ампулы по 15 мг.
НАБУМЕТОН (Релафен)
Подобно мелоксикаму селективно ингибирует ЦОГ-2. Быстро всасывается. Пища ускоряет всасывание. В печени образуется активный метаболит с периодом полувыведения примерно равным 24 часам.
Нежелательные реакции со стороны желудочно-кишечного тракта встречаются реже, чем при приеме других НПВС.
Показания
Ревматоидный артрит, остеоартроз.
Дозировка
Взрослые: 1000 мг один раз в день, в отдельных случаях 1500-2000 мг в день, в 1-2 приема, независимо от приема пищи.
Дети: дозы не установлены.
Форма выпуска:
– таблетки по 500 и 750 мг.
ИБУПРОФЕН (Бруфен, Мотрин)
По силе противовоспалительного действия уступает многим другим препаратам I группы. Однако при приеме ибупрофена в суточных дозах 1200 мг и выше достигается удовлетворительный противовоспалительный эффект. Анальгезирующее и жаропонижающее действия преобладают над противовоспалительной активностью.
Фармакокинетика
Максимальная концентрация в крови развивается через 1-2 часа после приема внутрь. Быстро метаболизируется и выводится из организма. Период полувыведения 1,8-2,5 часа, в силу этого, анальгетический и жаропонижающий эффекты поддерживаются до 8 часов. Достоинством препарата является хорошая переносимость, редкое развитие нежелательных реакций. Он является одним из наименее гастротоксичных среди НПВС.
Показания
Применяется чаще как анальгетик, а также при легких вариантах течения ревматоидного артрита, остеоартрозах.
В двойных слепых исследованиях получены данные об эффективности длительного применения ибупрофена в высоких дозах – 20-30 мг/кг (максимально 1600 мг) 2 раза в день в течение 4 лет – у больных муковисцидозом. Отмечено замедление прогрессирования легочной деструкции без серьезных нежелательных реакций (14).
Дозировка
Взрослые: по 400-600 мг 3-4 раза в день, препараты "ретард" – по 600-1200 мг 2 раза в день.
Дети: 20-40 мг/кг/день в 2-3 приема.
С 1995 года в США ибупрофен разрешен для безрецептурного применения у детей старше 2 лет при лихорадке и болевом синдроме по 7,5 мг/кг до 4 раз в день, максимально – 30 мг/кг/день.
Формы выпуска:
– таблетки по 200, 400 и 600 мг;
– таблетки "ретард" по 600, 800 и 1200 мг;
– крем, 5%.
НАПРОКСЕН (Напросин)
Одно из наиболее часто применяемых НПВС. По противовоспалительной активности превосходит ибупрофен. Противовоспалительный эффект развивается медленно, с максимумом через 2-4 недели. Обладает сильным анальгезирующим и жаропонижающим действием. Антиагрегационный эффект проявляется только при назначении высоких доз препарата. Не обладает урикозурическим действием.
Фармакокинетика
Хорошо всасывается при пероральном приеме и ректальном введении. Максимальная концентрация в крови отмечается через 2-4 часа после приема внутрь. Период полувыведения составляет около 15 часов, что позволяет назначать его 1-2 раза в день.
Нежелательные реакции
Гастротоксичность меньше, чем у индометацина, аспирина и пироксикама. Нефротоксичность отмечается, как правило, только у больных с почечной патологией и при сердечной недостаточности. Возможны аллергические реакции, описаны случаи перекрестной аллергии с аспирином.
Показания
Широко применяется при ревматизме, анкилозирующем спондилите, ревматоидном артрите у взрослых и детей. У больных с остеоартрозами он тормозит активность фермента протеогликаназы, предупреждая дегенеративные изменения суставного хряща, чем выгодно отличается от индометацина. Широко используется в качестве анальгетика, в том числе при послеоперационных и послеродовых болях, при гинекологических процедурах. Отмечена высокая эффективность при дисменорее, паранеопластической лихорадке.
Дозировка
Взрослые: 500-1000 мг/день в 1-2 приема внутрь или ректально. Суточная доза может быть увеличена до 1500 мг на ограниченный период (до 2 недель). При остром болевом синдроме (бурсит, тендовагинит, дисменорея) 1-я доза – 500 мг, затем по 250 мг каждые 6-8 часов.
Дети: 10-20 мг/кг/денъ в 2 приема. Как жаропонижающее – 15 мг/кг на прием.
Формы выпуска:
– таблетки по 250 и 500 мг;
– свечи по 250 и 500 мг;
– суспензия, содержащая 250 мг/5 мл;
– гель, 10%.
НАПРОКСЕН-НАТРИЙ (Алив, Апранакс)
Отличается от напроксена более быстрым всасыванием в желудочно-кишечном тракте и повышенной биодоступностью. Анальгезирующий эффект развивается уже через 15 минут, а максимальная концентрация в крови – через 1 час. Период полувыведения – 13 часов, что позволяет применять его не более 2 раз в день.
Показания
Прежде всего, применяется как быстродействующий анальгетик при головной и зубной боли, послеоперационных болях, травмах, дисменорее. Для безрецептурного применения выпускается под названием олив. По противовоспалительной активности равен напроксену, поэтому может быть использован в ревматологии.
Дозировка
Взрослые: по 220-550 мг 1-2 раза в день.
Дети: 10-20 мг/кг/день в 2 приема.
Форма выпуска:
– таблетки по 220 мг (Алив), 275 и 550 мг (Апранакс).
ФЛУРБИПРОФЕН (Ансейд, Флугалин, Фробен)
По фармакодинамике близок к напроксену. Нежелательные реакции, особенно со стороны желудочно-кишечного тракта, кожные сыпи, бронхоспазм отмечаются несколько чаще, чем при назначении напроксена. Максимальная концентрация в крови развивается через 1,5 часа после приема внутрь. Период полувыведения варьирует у различных больных от 3 до 9 часов.
Дозировка
Взрослые: по 50-100 мг 3-4 раза в день.
Дети: 4 мг/кг/день в 2-4 приема.
Формы выпуска:
– таблетки по 50 и 100 мг;
– свечи по 100 мг.
КЕТОПРОФЕН (Кетонал, Кнавон, Орудие, Профенид)
Обладает выраженным противовоспалительным и анальгезируюшим действием. Контролируемые клинические исследования у больных ревматоидным артритом и остеоартрозом показали, что он не уступает по эффективности индометацину, диклофенаку и напроксену, превосходя ибупрофен и пироксикам. В дозе 50-100 мг кетопрофен оказывает более сильный анальгезирующий эффект, чем комбинации парацетамол/кодеин и аспирин/кодеин.
Фармакокинетика
Хорошо всасывается при различных путях введения. Максимальная концентрация в крови развивается через 1-2 часа после приема внутрь, через 2,4-4 часа после ректального и через 15-20 минут после внутримышечного введения. Период полувыведения составляет 1,6-1,9 часов.
Нежелательные реакции
В основном, со стороны желудочно-кишечного тракта в виде диспептических и диспепсических расстройств. В редких случаях отмечаются нарушения функции почек и печени, головная боль, шум в ушах, зрительные расстройства. Возможны аллергические реакции.
Показания
Ревматоидный артрит, подагрический артрит, остеоартроз, болевой синдром (дисменорея, почечная колика, послеоперационные и посттравматические боли, боли при онкологических заболеваниях). При острой закрытой травме мягких тканей кетопрофен может использоваться наружно в виде геля. Как показали контролируемые исследования, он превосходит по эффективности аналогичные лекарственные формы диклофенака и пироксикама. При сильных болях кетопрофен может использоваться в комбинации с наркотическими анальгетиками.
Дозировка
Взрослые:
внутрь и ректально 100-300 мг/сутки в 2-3 приема, причем прием таблеток или капсул можно сочетать с использованием свечей, например, 1 капсула (50 мг) утром и днем и 1 свеча (100 мг) вечером,
внутримышечно – по 100 мг 1-2 раза в сутки;
внутривенно – кратковременная инфузия – 100-200 мг в 100 мл физиологического раствора натрия хлорида в течение 0,5-1 часа каждые 8 часов;
длительная инфузия – 100-200 мг в 500 мл физиологического раствора натрия хлорида (или раствора глюкозы) в течение 8 часов с 8-часовыми интервалами, при длительной инфузии кетопрофен можно смешивать с 10-20 мл морфина, но нельзя смешивать с трамадолом, так как выпадает осадок.
Дети: дозы не установлены.
Формы выпуска:
– таблетки по 50, 100 и 150 ("ретард") мг; – капсулы по 50 мг; – свечи по 100 мг; – ампулы по 2 мл (100 мг); – гель, 5%.
ТИАПРОФЕНОВАЯ КИСЛОТА (Сургам)
По противовоспалительной активности близка к напроксену. Обладает выраженным анальгезирующим действием. Быстро всасывается при приеме внутрь. Максимальная концентрация в крови развивается через 1 час. Период полувыведения 3 часа. Имеются данные о положительном влиянии препарата на метаболизм суставного хряща.
Нежелательные реакции
Может вызывать раздражение слизистой оболочки мочевого пузыря вплоть до развития цистита, что проявляется гематурией и дизурическими явлениями. Поэтому не следует использовать тиапрофеновую кислоту у пациентов с заболеваниями мочевыводящих путей и предстательной железы (включая указания на них в анамнезе).
Дозировка
Взрослые: по 300 мг 2 раза в день. У больных с почечной, печеночной и сердечной недостаточностью – 200 мг 2 раза в день.
Дети: дозы не установлены.
Формы выпуска:
– таблетки по 100 и 300 мг;
– свечи по 150 и 300 мг.
ФЕНОПРОФЕН (Налфон)
По противовоспалительной активности близок к напроксену, по анальгетической – к аспирину. Максимальная концентрация в крови развивается через 2 часа после приема внутрь. Период полувыведения составляет около 3 часов.
Дозировка
Взрослые: по 200-300 мг 3-4 раза в день.
Дети: дозы не установлены.
Форма выпуска:
– таблетки по 200 и 300 мг.
ЦЕЛЕКОКСИБ (Целебрекс)
Препарат из группы некислотных производных (является производным сульфонамида). Представитель нового поколения НПВС – селективных ингибиторов ЦОГ-2. В связи с этим избирательно нарушает образование простагландинов, участвующих в формировании воспалительной реакции, и не влияет на продукцию простагландинов, регулирующих почечный кровоток и целостность слизистой оболочки ЖКТ. Не нарушает синтез тромбоксана, поэтому не влияет на агрегацию тромбоцитов. Обладает выраженным противовоспалительным и анальгезирующим действием.
Фармакокинетика
Хорошо всасывается в ЖКТ, пиковая концентрация в крови развивается через 3 ч. Пища, особенно жирная, замедляет скорость всасывания, но при этом несколько увеличивает его объем (на 10-20%). Метаболизируется в печени, экскретируется со стулом (преимущественно) и с мочой. Т1/2 – 11 ч, может возрастать при среднетяжелых нарушениях функции печени.
Нежелательные реакции
Являясь селективным ингибитором ЦОГ-2, целекоксиб значительно реже, чем другие НПВС, вызывает нежелательные реакции со стороны ЖКТ. При этом частота возникновения язв желудка и 12-перстной кишки не отличается от плацебо, а кровотечения и перфорации не наблюдаются. Могут отмечаться головная боль, головокружение, нарушения сна, сыпи, явления ринита. Нефротоксических реакций не зарегистрировано.
Лекарственные взаимодействия
Флуконазол в 2 раза повышает концентрацию целекоксиба в плазме крови за счет ингибирования его метаболизма в печени.
Целекоксиб увеличивает концентрацию лития в плазме.
Не установлено взаимодействий целекоксиба с диуретиками, антигипертензивными ЛС, непрямыми антикоагулянтами, метотрексатом.
Показания
Ревматоидный артрит, остеоартроз.
Дозировка
Взрослые: внутрь – 100-200 мг/день в 1-2 приема.
Дозы для детей до 18 лет не установлены.
Формы выпуска
Капсулы по 100 и 200 мг.
НПВС СО СЛАБОЙ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ
Препараты данной группы сочетают выраженное анальгезирующее и жаропонижающее действие со слабым противовоспалительным эффектом. Поэтому они не применяются в качестве противовоспалительных, используются как анальгетики и антипиретики.
МЕФЕНАМОВАЯ (МЕФЕНАМИНОВАЯ) КИСЛОТА (Понстел)
По противовоспалительному эффекту значительно уступает препаратам I группы. Используется как анальгетик и антипиретик. Курс лечения не должен превышать 1 неделю.
Фармакокинетика
Медленно всасывается в желудочно-кишечном тракте, частично метаболизируется в печени, период полувыведения – 4 часа.
Нежелательные реакции
Часто вызывает нежелательные реакции (у 25% больных), особенно со стороны желудочно-кишечного тракта. Характерной является диарея, сопряженная с воспалением толстого кишечника. Обладает гепатотоксичностыо, может вызывать гемолитическую анемию, аллергические реакции. У пожилых возможно развитие неолигурической почечной недостаточности, особенно при обезвоживании.
Дозировка
Взрослые: первая доза – 500 мг, далее по 250 мг 4 раза в день.
Дети: старше 14 лет – разовая доза 6,5 мг/кг.
У детей до 14 лет не применяется.
Формы выпуска:
– таблетки по 500 мг;
– сироп.
ЭТОФЕНАМАТ (Реймон гель, Этогель)
Препарат для наружного применения. Оказывает местное противовоспалительное и анальгезирующее действие.
Показания
Бурсит, тендовагинит, суставной синдром, миозит, люмбаго, растяжения, вывихи, ушибы.
Дозировка
Столбик геля 5-10 см наносится на область поражения и медленно втирается 2-3 раза в день.
Предупреждения
Нельзя наносить на поврежденную кожу.
Форма выпуска:
– гель, 5%.
МЕТАМИЗОЛ
(Анальгин, Баралгин М, Девалгин, Новалгин, Торалгин)
В некоторых странах используется под генерическим названием дипирон. Несмотря на структурное сходство с фенилбутазоном, обладает значительно меньшим противовоспалительным действием. Это объясняется слабым влиянием метамизола на синтез ПГ в очагах воспаления. Обладает выраженным анальгезирующим эффектом, который обусловлен, преимущественно, центральными механизмами, в частности, нарушением проведения болевых импульсов в спинном мозге. В отличие от других НПВС обладает спазмолитической активностью.
Фармакокинетика
Быстро и практически полностью всасывается. Максимальная концентрация в крови развивается через 1-2 часа. Период полувыведения – 2,5 часа.
Нежелательные реакции
Необходимо помнить об опасности развития гематологических осложнений, свойственных всем пиразолонам и пиразолидинам, и соблюдать меры предосторожности (табл. 7).
Показания
Применяется как анальгетик и антипиретик. Для оказания быстрого эффекта вводится парентерально.
Дозировка
Взрослые: внутрь по 0,5-1 г 3-4 раза в день, внутримышечно или внутривенно по 2-5 мл 50% р-ра 2-4 раза в день.
Дети: по 5-10 мг/кг 3-4 раза в день. При гипертермии внутривенно или внутримышечно в виде 50% р-ра: до 1 года – 0,01 мл/кг, старше 1 года – 0,1 мл/год жизни на одно введение.
Формы выпуска:
– таблетки по 100 и 500 мг;
– ампулы по 1 мл 25% р-ра, 1 и 2 мл 50% р-ра;
– капли, сироп, свечи.
АМИНОФЕНАЗОН (Амидопирин)
В течение многих лет применялся в качестве анальгетика и антипиретика. Более токсичен, чем метамизол. Чаще вызывает тяжелые кожные аллергические реакции, особенно при сочетании с сульфаниламидами. В настоящее время аминофеназон запрещен к использованию и снят с производства, так как при взаимодействии с нитритами пищи может приводить к образованию канцерогенных соединений.
Несмотря на это в аптечную сеть продолжают поступать препараты, содержащие аминофеназон (омазол, анапирин, пенталгин, пирабутол, пиранал, пиркофен, реопирин, теофедрин Н).
ПРОПИФЕНАЗОН
Обладает выраженным анальгезирующим и жаропонижающим действием. Быстро всасывается в желудочно-кишечном тракте, максимальная концентрация в крови развивается через 30 минут после приема внутрь.
По сравнению с другими производными пиразолона наиболее безопасен. При его применении не отмечено развития агранулоцитоза. В редких случаях наблюдается снижение числа тромбоцитов и лейкоцитов.
В виде монопрепарата не используется, входит в состав комбинированных препаратов саридон и пливалгин.
ФЕНАЦЕТИН
Фармакокинетика
Хорошо всасывается в желудочно-кишечном тракте. Метаболизируется в печени, частично превращаясь в активный метаболит парацетамол. Другие метаболиты фенацетина токсичны. Период полувыведения составляет 2-3 часа.
Нежелательные реакции
Фенацетин обладает высокой нефротоксичностью. Он может вызывать тубулоинтерстициальный нефрит, обусловленный ишемическими изменениями в почках, которые проявляются болями в пояснице, дизурическими явлениями, гематурией, протеинурией, цилиндрурией ("анальгетическая нефропатия", "фенацетиновая почка"). Описано развитие тяжелой почечной недостаточности. Нефротоксические эффекты в большей степени проявляются при длительном применении в сочетании с другими анальгетиками, чаще отмечаются у женщин.
Метаболиты фенацетина могут вызывать образование метгемоглобина и гемолиз. У препарата выявлены также канцерогенные свойства: он может вести к развитию рака мочевого пузыря.
Во многих странах фенацетин запрещен к применению.
Дозировка
Взрослые: по 250-500 мг 2-3 раза в день.
У детей не применяется.
Формы выпуска:
Входит в состав различных комбинированных препаратов: таблетки пиркофен, седалгин, теофедрин Н, свечи цефекон.
ПАРАЦЕТАМОЛ
(Калпол, Лекадол, Мексален, Панадол, Эффералган)
Парацетамол (в некоторых странах имеет генерическое название ацетаминофен) – активный метаболит фенацетина. По сравнению с фенацетином менее токсичен.
Больше подавляет синтез простагландинов в центральной нервной системе, чем в периферических тканях. Поэтому оказывает преимущественно "центральное" анальгезирующее и жаропонижающее действие и имеет очень слабую "периферическую" противовоспалительную активность. Последняя может проявляться только при низком содержании в тканях перекисных соединений, например, при остеоартрозе, при острой травме мягких тканей, но не при ревматических заболеваниях.
Фармакокинетика
Парацетамол хорошо всасывается при приеме внутрь и ректальном введении. Максимальная концентрация в крови развивается через 0,5-2 часа после приема. У вегетарианцев всасывание парацетамола в желудочно-кишечном тракте значительно ослаблено. Препарат метаболизируется в печени в 2 стадии: сначала под действием ферментных систем цитохрома Р-450 образуются промежуточные гепатотоксичные метаболиты, которые затем расщепляются при участии глютатиона. Менее 5% введенного парацетамола экскретируется в неизмененном виде почками. Период полувыведения – 2-2,5 часа. Продолжительность действия – 3-4 часа.
Нежелательные реакции
Парацетамол считается одним из наиболее безопасных НПВС. Так, в отличие от аспирина, он не вызывает синдром Рея, не обладает гастротоксичностыо, не влияет на агрегацию тромбоцитов. В отличие от метамизола и фенилбутазона не вызывает агранулоцитоз и апластическую анемию. Аллергические реакции на парацетамол наблюдаются редко.
Недавно получены данные, что при длительном приеме парацетамола более 1 таблетки в день (1000 и более таблеток за жизнь) вдвое увеличивается риск развития тяжелой анальгетической нефропатии, приводящей к терминальной почечной недостаточности (15). В основе лежит нефротоксическое действие метаболитов парацетамола, особенно парааминофенола, который накапливается в почечных сосочках, связывается с SH-группами, вызывая тяжелые нарушения функции и структуры клеток, вплоть до их гибели. В то же время, систематический прием аспирина не связан с подобным риском. Таким образом, парацетамол более нефротоксичен, чем аспирин, и не следует считать его "абсолютно безопасным" препаратом.
Следует также помнить о гепатотоксичности парацетамола при приеме в очень больших (!) дозах. Одномоментный прием его в дозе более 10 г у взрослых или более 140 мг/кг у детей ведет к отравлению, сопровождающемуся тяжелым поражением печени. Причина – истощение запасов глютатиона и накопление промежуточных продуктов метаболизма парацетамола, обладающих гепатотоксическим действием. Симптоматика отравления разделяется на 4 стадии (табл. 10).
Таблица 10. Симптомы интоксикации парацетамолом. (По Merck Manual, 1992) [16]
| Стадия | Срок | Клиника |
|---|---|---|
| I | Первые 12-24 ч. | Лёгкие симптомы раздражения ЖКТ. Пациент не чувствует себя больным. |
| II | 2-3 дня | Симптомы со стороны ЖКТ, особенно тошнота и рвота; увеличение АСТ, АЛТ, билирубина, протромбинового времени. |
| III | 3-5 дней | Неукротимая рвота; высокие значения АСТ, АЛТ, билирубина, протромбинового времени; признаки печёночной недостаточности. |
| IV | Спустя 5 дней | Восстановление функции печени или смерть от печёночной недостаточности. |
Подобная картина может наблюдаться и при приеме обычных доз препарата в случае сопутствующего применения индукторов ферментов цитохрома Р-450, а также у алкоголиков (см. ниже).
Меры помощи при интоксикации парацетамолом представлены в табл. 11. Необходимо иметь в виду, что форсированный диурез при отравлении парацетамолом малоэффективен и даже опасен, перитонеальный диализ и гемодиализ неэффективны. Ни в коем случае нельзя применять антигистаминные препараты, глюкокортикоиды, фенобарбитал и этакриновую кислоту, которые могут оказать индуцирующее влияние на ферментные системы цитохрома Р-450 и усилить образование гепатотоксичных метаболитов.
Взаимодействия
Всасывание парацетамола в желудочно-кишечном тракте усиливают метоклопрамид и кофеин.
Индукторы печеночных ферментов (барбитураты, рифампицин, дифенин и другие) ускоряют расщепление парацетамола до гепатотоксичных метаболитов и увеличивают риск поражений печени.
Таблица 11. Меры помощи при интоксикации парацетамолом
- Промывание желудка.
- Активированный угль внутрь.
- Вызывание рвоты.
- Ацетилцистеин (является донатором глютатиона) – 20% раствор внутрь.
- Глюкоза внутривенно.
- Витамин K1 (фитоменадион) – 1-10 мг внутримышечно, нативная плазма, факторы свертывания крови (при 3-кратном увеличении протромбинового времени).
Подобные эффекты могут наблюдаться у лиц, систематически употребляющих алкоголь. У них гепатотоксичность парацетамола отмечается даже при использовании в терапевтических дозах (2,5-4 г/сутки), особенно если он принимается через короткий промежуток времени после алкоголя (8).
Показания
В настоящее время парацетамол рассматривается как эффективный аналъгетик и антипиретик для широкого применения. Он в первую очередь рекомендуется при наличии противопоказаний к аспирину и другим НПВС: у больных бронхиальной астмой, у лиц с язвенным анамнезом, у детей с вирусными инфекциями. По анальгезирующей и жаропонижающей активности парацетамол близок к аспирину.
Предупреждения
Парацетамол должен с осторожностью применяться у больных с нарушениями функций печени и почек, а также у тех, которые принимают препараты, влияющие на функцию печени.
Дозировка
Взрослые: по 500-1000 мг 4-6 раз в день.
Дети: по 10-15 мг/кг 4-6 раз в день.
Формы выпуска:
– таблетки по 200 и 500 мг;
– сироп 120 мг/5 мл и 200 мг/5 мл;
– свечи по 125, 250, 500 и 1000 мг;
– "шипучие" таблетки по 330 и 500 мг. Входит в состав комбинированных препаратов соридон, солпадеин, томапирин, цитрамон П и других.
КЕТОРОЛАК (Торадол, Кетродол)
Основная клиническая ценность препарата – его мощный анальгезирующий эффект, по степени которого он превосходит многие другие НПВС.
Установлено, что 30 мг кеторолака, введенного внутримышечно, примерно эквивалентны 12 мг морфина. В то же время, нежелательные реакции, характерные для морфина и других наркотических анальгетиков (тошнота, рвота, угнетение дыхания, запоры, задержка мочи), отмечаются значительно реже. Применение кеторолака не ведет к развитию лекарственной зависимости.
Кеторолак обладает также жаропонижающим и антиагрегационным действием.
Фармакокинетика
Практически полностью и быстро всасывается в желудочно-кишечном тракте, биодоступность при приеме внутрь составляет 80-100%. Максимальная концентрация в крови развивается через 35 минут после приема внутрь и через 50 минут после введения внутримышечно. Выводится почками. Период полувыведения 5-6 часов.
Нежелательные реакции
Наиболее часто отмечаются гастротоксичность и повышенная кровоточивость, обусловленная антиагрегационным действием.
Взаимодействие
При сочетании с опиоидными анальгетиками болеутоляющий эффект усиливается, что дает возможность применять их в более низких дозах.
Внутривенное или внутрисуставное введение кеторолака в сочетании с местными анестетиками (лидокаин, бупивакаин) обеспечивает лучшее обезболивание, чем применение только одного из препаратов, после артроскопии и операциях на верхних конечностях.
Показания
Используется для купирования болевого синдрома различной локализации: почечной колики, болей при травмах, при неврологических заболеваниях, у онкологических больных (особенно при метастазах в костях), в послеоперационном и послеродовом периоде.
Появились данные о возможности применения кеторолака перед операциями в сочетании с морфином или фентанилом. Это позволяет снижать дозы опиоидных анальгетиков на 25-50% в первые 1-2 суток послеоперационного периода, что сопровождается более быстрым восстановлением функции желудочно-кишечного тракта, меньшей тошнотой и рвотой и сокращает срок пребывания больных в стационаре (17).
Применяется также для обезболивания в оперативной стоматологии и при ортопедических лечебных процедурах.
Предупреждения
Нельзя применять кеторолак перед длительными операциями с высоким риском кровотечений, а также для поддерживающей анестезии во время операций, для обезболивания родов, купирования болевого синдрома при инфаркте миокарда.
Курс применения кеторолака не должен превышать 7 дней, а у лиц старше 65 лет препарат должен назначаться с осторожностью.
Дозировка
Взрослые: внутрь 10 мг каждые 4-6 часов; высшая суточная доза – 40 мг; продолжительность применения не более 7 дней. Внутримышечно и внутривенно – 10-30 мг; высшая суточная доза – 90 мг; продолжительность применения не более 2 дней.
Дети: внутривенно 1-я доза – 0,5-1 мг/кг, затем 0,25-0,5 мг/кг каждые 6 часов.
Формы выпуска:
– таблетки по 10 мг;
– ампулы по 1 мл.
КОМБИНИРОВАННЫЕ ПРЕПАРАТЫ
Выпускается целый ряд комбинированных препаратов, содержащих кроме НПВС другие лекарственные средства, которые, благодаря своим специфическим свойствам, могут усиливать анальгезирующий эффект НПВС, повышать их биодоступность и уменьшать риск нежелательных реакций.
САРИДОН
Состоит из парацетамола, пропифеназона и кофеина. Соотношение анальгетиков в препарате составляет 5:3, при котором они действуют как синергисты, так как парацетамол в данном случае в полтора раза увеличивает биодоступность пропифеназона. Кофеин нормализует тонус сосудов головного мозга, ускоряет кровоток, не стимулируя в используемой дозе центральную нервную систему, поэтому он усиливает действие анальгетиков при головной боли. Помимо этого, он улучшает всасывание парацетамола. Саридон, в целом, характеризуется высокой биодоступностью и быстрым развитием анальгезирующего эффекта.
Показания
Болевой синдром различной локализации (головная боль, зубная боль, боль при ревматических заболеваниях, дисменорея, лихорадка).
Дозировка
По 1-2 таблетки 1-3 раза в день.
Форма выпуска:
– таблетки, содержащие по 250 мг парацетамола, 150 мг пропифеназона и 50 мг кофеина.
ТОМАПИРИН
Препарат, состоящий из аспирина, парацетамола и кофеина. Применяется при головной боли, невралгиях, дисменорее, лихорадке.
Дозировка
По 1-1,5 таблетки 1-3 раза в день.
Форма выпуска:
– таблетки, содержащие по 250 мг аспирина, 200 мг парацетамола и 50 мг кофеина.
ТОМАПИРИН С
Выпускается в виде "шипучих" таблеток, каждая из которых содержит 300 мг аспирина, по 200 мг парацетамола и аскорбиновой кислоты. Показания к применению и дозировка такие же, как у томапирина.
ЦИТРАМОН П
Активные компоненты препарата – аспирин, парацетамол и кофеин – взаимно усиливают действие друг друга. Он применяется, в основном, при головной боли.
Дозировка
По 1-2 таблетки 1-3 раза в день.
Форма выпуска:
– таблетки, содержащие по 240 мг аспирина, 180 мг парацетамола и 30 мг кофеина.
АЛКА-ЗЕЛЬТЦЕР
Состав: аспирин, лимонная кислота, натрия бикарбонат. Представляет собой хорошо усваиваемую растворимую лекарственную форму аспирина с улучшенными органолептическими свойствами. Натрия бикарбонат нейтрализует в желудке свободную соляную кислоту, уменьшая ульцерогенное действие аспирина. Кроме того, он может усиливать всасывание аспирина.
Применяется, главным образом, при головной боли, особенно у лиц с повышенной кислотностью в желудке.
Дозировка
По 1-2 таблетки 3-4 раза в день.
Форма выпуска:
– "шипучие" таблетки, содержащие по 324 мг аспирина, 965 мг лимонной кислоты и 1625 мг натрия бикарбоната.
ФОРТАЛГИН Ц
Препарат представляет собой "шипучие" таблетки, каждая из которых содержит 400 мг аспирина и 240 мг аскорбиновой кислоты. Применяется как анальгетик и антипиретик.
Дозировка
По 1-2 таблетки до четырех раз в день.
ПЛИВАЛГИН
Выпускается в виде таблеток, каждая из которых содержит по 210 мг парацетамола и пропифеназона, 50 мг кофеина, 25 мг фенобарбитала и 10 мг кодеина фосфата. Анальгезирующий эффект препарата усилен за счет наличия наркотического анальгетика кодеина и фенобарбитала, обладающего седативным действием. Роль кофеина рассмотрена выше.
Показания
Боли различной локализации (головная, зубная, мышечная, суставная, невралгия, дисменорея), лихорадка.
Предупреждения
При частом использовании, особенно в повышенной дозе, может возникать чувство усталости, сонливости. Возможно развитие лекарственной зависимости.
Дозировка
По 1-2 таблетки 3-4 раза в день.
РЕОПИРИН (Пирабутол)
В состав входят аминофеназон (амидопирин) и фенилбутазон (бутадион). В течение многих лет широко применялся в качестве анальгетика. Однако он не имеет преимуществ по эффективности перед современными НПВС и существенно превосходит их по тяжести нежелательных реакций. Особенно высок риск развития гематологических осложнений, поэтому необходимо соблюдать все указанные выше меры предосторожности (табл. 7) и стремиться использовать другие анальгетики. При внутримышечном введении фенилбутазон связывается тканями в месте инъекции и плохо рассасывается, что, во-первых, задерживает развитие эффекта и, во-вторых, является причиной частого развития инфильтратов, абсцессов, поражений седалищного нерва.
В настоящее время применение комбинированных препаратов, состоящих из фенилбутазона и аминофеназона, в большинстве стран запрещено.
Дозировка
Взрослые: внутрь по 1-2 таблетки 3-4 раза в день, внутримышечно 2-3 мл 1-2 раза в день.
У детей не применяется.
Формы выпуска:
– таблетки, содержащие по 125 мг фенилбутазона и аминофеназона;
– ампулы по 5 мл, содержащие по 750 мг фенилбутазона и аминофеназона.
БАРАЛГИН
Представляет собой комбинацию метамизола (анальгина) с двумя спазмолитиками, один из которых – питофенон – обладает миотропным, а другой – фенпивериниум – атропиноподобным действием. Применяется для купирования болей, обусловленных спазмом гладкой мускулатуры (почечная колика, печеночная колика и другие). Как и другие лекарственные средства, обладающие атропиноподобной активностью, противопоказан при глаукоме и аденоме простаты.
Дозировка
Внутрь по 1-2 таблетки 3-4 раза в день, внутримышечно или внутривенно по 3-5 мл 2-3 раза в день. Внутривенно вводят со скоростью 1-1,5 мл в минуту.
Формы выпуска:
– таблетки, содержащие по 500 мг метамизола, 10 мг питофенона и 0,1 мг фенпивериниума;
– ампулы по 5 мл, содержащие по 2,5 г метамизола, 10 мг питофенона и 0,1 мг фенпивериниума.
АРТРОТЕК
Состоит из диклофенака и мизопростола (синтетический аналог ПГ-E1), включение которого преследует цель уменьшить частоту и выраженность нежелательных реакций, характерных для диклофенака, в особенности, гастротоксичности. Артротек по эффективности при ревматоидном артрите и остеоартрозе равноценен диклофенаку, а развитие эрозий и язв желудка при его использовании отмечается значительно реже.
Дозировка
Взрослые: по 1 таблетке 2-3 раза в день.
Форма выпуска:
– таблетки, содержащие по 50 мг диклофенака и 200 мг мизопростола.
СПИСОК ЛИТЕРАТУРЫ
- Champion G.D, Feng P.H„ Azuma T. et al. NSAID-induced gastrointestinal damage // Drugs, 1997, 53: 6-19.
- Laurence D.R., Bennett P.N. Clinical Pharmacology. 7th ed. Churcill Livingstone. 1992.
- Insel P.A. Analgesic-antipyretic and antiinflammatory agents and drugs employed in the treatment of gout. In: Goodman & Gilman's. The pharmacological basis of therapeutics. 9th ed. McGraw-Hill, 1996, 617-657.
- Нестероидные противовоспалительные средства. (Редакц. статья) // Клин. фармакол. и фармакотер., 1994, 3, 6-7.
- Loeb D.S., Ahlquist D.A., Talley N.J. Management of gastroduo-denopathy associated with use of nonsteroidal anti-inflammatory drugs // Mayo Clin. Proc., 1992, 67: 354-364.
- Espinosa L., Lipani J., Poland M., Wallin B. Perforations, ulcers and bleeds in a large, randomized, multicenter trial of namubetone compared with diclofenac, ibuprofen, naproxen and piroxicam // Rev. Esp. Reumatol., 1993, 20 (suppl. I): 324.
- Brooks P.M., Day R.O. Nonsteroidal antiinfla mmatory drugs – differences and similarities // N. Engl. J. Med., 1991, 324: 1716-1725.
- Lieber C.S. Medical disorders of alcoholism // N. Engl. J. Med., 1995, 333: 1058-1065.
- Guslandi M. Gastric toxicity of antiplatelet therapy with low-dose aspirin // Drugs, 1997, 53: 1-5.
- Applied Therapeutics: The clinical use of drugs. 6th ed. Young L.Y., Koda-Kimble M.A. (Eds). Vancouver. 1995.
- Drugs of choice from the Medical Letter. New York. Revised ed. 1995.
- Marcus A.L. Aspirin as prophilaxis against colorectal cancer // N. Engl.J. Med.,1995, 333: 656-658
- Noble S, Balfour J. Meloxicam // Drugs, 1996, 51: 424-430.
- Konstan M.W., Byard PJ., Hoppel C.L., Davis P.B. Effect of high dose ibuprofen in patients with cystic fibrosis // N. Engl. J. Med., 1995, 332: 848-854.
- Perneger T.V., Whelton P.К., Klag MJ. Risk of kidney failure associated with the use of acetaminophen, aspirin, and nonsteroidal anti-inflammatory drugs // N. Engl. J. Med, 1994, 331: 1675-1712.
- Merck Manual of Diagnosis and Therapy. 16th ed. Berkow R. (Ed.). Merck & Co Inc., 1992.
- Gillis J.C., Brogden R.N. Ketorolak. A reappraisal of its pharmacodinamic and pharmacokinetic properties and therapeutic use in pain management // Drugs, 1997, 53: 139-188.